
科目: 来源: 题型:选择题
| A. | 三硫代碳酸钾 | B. | 多硫碳化钾 | C. | 过硫碳酸钾 | D. | 超硫碳酸钾 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CO2 | B. | N2 | C. | SO2 | D. | CO |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验所用试剂或操作 | 实 验 现 象 | 验证的性质 |
| 碘化钾淀粉溶液 | ||
| 取适量过氧化氢溶液于试管中,加热,用带火星的木条检验. |
查看答案和解析>>
科目: 来源: 题型:解答题
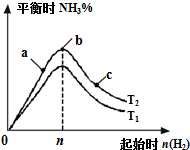 某科研小组研究在其他条件不变的情况下,改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol 反应的影响,实验结果可表示成如图所示的规律(T表示温度,n表示物质的量):
某科研小组研究在其他条件不变的情况下,改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol 反应的影响,实验结果可表示成如图所示的规律(T表示温度,n表示物质的量):查看答案和解析>>
科目: 来源: 题型:推断题
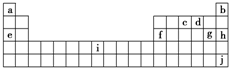
 A、B、C、D、E、F、G、H、I、J有如图所示的转化关系.图中所有物质均由短周期元素组成,且每个小三角形内的三种物质均至少含有第三周期中的一种相同元素.其它信息见表:
A、B、C、D、E、F、G、H、I、J有如图所示的转化关系.图中所有物质均由短周期元素组成,且每个小三角形内的三种物质均至少含有第三周期中的一种相同元素.其它信息见表:| 编号 | 信息 | 编号 | 信息 |
| 1 | D为地壳中含量最高的元素组成的单质 | 4 | H为淡黄色固体化合物 |
| 2 | E为酸性气态氧化物 | 5 | 电解饱和J溶液是工业重要反应 |
| 3 | F的浓溶液常做干燥剂 | 6 | C为离子化合物,阴、阳离子均含金属元素 |
 .
.查看答案和解析>>
科目: 来源: 题型:解答题
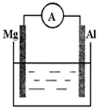 如图所示装置:
如图所示装置:查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:推断题

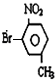 或
或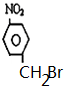 .
. (注明反应条件).
(注明反应条件). .
.查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com