
科目: 来源: 题型:选择题
| A. | 制氧气时,用Na2O2或H2O2做反应物可选择相同的气体发生装置 | |
| B. | 制氯气时,用饱和NaHCO3和浓硫酸净化气体 | |
| C. | 制氨气时,用排水法或向上排空气法收集气体 | |
| D. | 制二氧化氮时,用水或NaOH溶液吸收尾气 |
查看答案和解析>>
科目: 来源: 题型:实验题
 如图是某同学设计的放热反应的观察装置,其实验操作步骤如下①按图所示将实验装置连接好;②在U形管内加入少量红墨水(或品红溶液),打开T形管活塞,使U形管内两边的液面处于同一水平面,再关闭T形管活塞;③在盛有1g氧化钙的小试管里滴入2mL左右的蒸馏水,观察现象.
如图是某同学设计的放热反应的观察装置,其实验操作步骤如下①按图所示将实验装置连接好;②在U形管内加入少量红墨水(或品红溶液),打开T形管活塞,使U形管内两边的液面处于同一水平面,再关闭T形管活塞;③在盛有1g氧化钙的小试管里滴入2mL左右的蒸馏水,观察现象.查看答案和解析>>
科目: 来源: 题型:实验题
| 选用试剂 | 实验现象 | |
| 方案1 | ||
| 方案2 |
查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 萃取剂要求不溶于水,且比水更容易使碘溶解 | |
| B. | 注入碘水和萃取剂,倒转分液漏斗反复用力振荡后立即分液 | |
| C. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| D. | 实验室如果没有四氯化碳,可以用酒精代替 |
查看答案和解析>>
科目: 来源: 题型:解答题
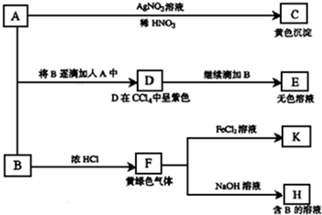
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加热 | B. | 不用稀硫酸,改用98%浓硫酸 | ||
| C. | 加入硫酸铜 | D. | 不用铁片,改用铁粉 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 碱性溶液:Cu2+、Al3+、NO3-、SO42- | |
| B. | 加入KSCN显红色的溶液:K+、NH4+、Cl-、I- | |
| C. | 加入Al能放出大量H2的溶液中:NH4+、Fe2+、NO3-、SO42- | |
| D. | 常温下,c(H+)/c(OH一)=1×10-12的溶液:K+、AlO2-、CO32-、Na+ |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com