
科目: 来源: 题型:解答题
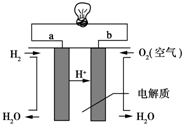
查看答案和解析>>
科目: 来源: 题型:实验题
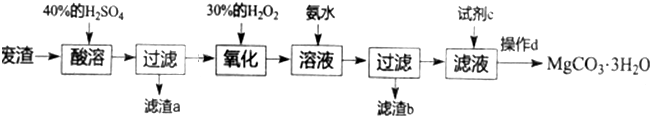
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na、Mg、Al元素最高化合价依次升高 | |
| B. | P、Cl最高价氧化物对应的水化物酸性增强 | |
| C. | N、O、F元素非金属性依次减弱 | |
| D. | Li、Na、K原子的电子层数依次增多 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
| 草酸 | 碳酸 | |
| 一级电离常数(Kad) | 5.9×10-2 | 4.2×10-7 |
| 二级电离常数(Kad) | 6.4×10-3 | 5.6×10-11 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | K+、Fe2+、NO3-、Cl-- | B. | K+、Al3+、SO42-、Cl- | ||
| C. | K+、NH4+、SO42-、Cl- | D. | Na+、K+、Br-、AlO2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com