
科目: 来源: 题型:选择题
| A. | 除去苯中的少量苯酚:加浓溴水,过滤 | |
| B. | 除去乙酸乙酯中的少量乙酸:加入饱和Na2CO3溶液,过滤 | |
| C. | 除去甲醛中少量的乙烯:通过盛有溴水的洗气瓶,洗气 | |
| D. | 除去溴苯中少量的Br2:加入稍过量氢氧化钠,分液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甲酸甲酯的结构简式:C2H4O2 | B. | 乙醛分子的比例模型: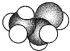 | ||
| C. | 聚对羟基苯甲酸酯的结构简式: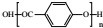 | D. | 丙烷分子的球棍模型: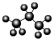 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 用锌粒代替锌粉 | B. | 向其中加入少量1mol/L硫酸溶液 | ||
| C. | 向其中加入氯化钠溶液 | D. | 向其中加入等体积的水 | ||
| E. | 向其中加入碳酸钠溶液 | F. | 向其中加入硝酸钠溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | A、B两种元素可组成化学式为BA2的化合物 | |
| B. | F与D形成的化合物性质很不活泼,不与任何酸反应 | |
| C. | 原子半径由大到小的顺序是E>F | |
| D. | 气态氢化物的稳定性由强到弱的顺序是C>D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用激光笔鉴别淀粉溶液与氯化钠溶液 | |
| B. | 用KOH溶液鉴别NH4Cl、AlCl3、MgSO4、FeCl3四种溶液 | |
| C. | 用盐酸溶液鉴别Na2CO3溶液和Na2SiO3溶液 | |
| D. | 用BaCl2溶液鉴别AgNO3和Na2SO4 |
查看答案和解析>>
科目: 来源: 题型:解答题
 实验室有一份混有碳酸钙杂质的碳酸钡样品.分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):
实验室有一份混有碳酸钙杂质的碳酸钡样品.分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com