
科目: 来源: 题型:实验题

| 平行试验次数 | 1 | 2 | 3 |
| 0.25g样品消耗硫酸铈标准溶液的体积(ml) | 24.35 | 24.05 | 23.95 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 元 素 | Mn | Fe | |
| 电离能 (kJ•mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
查看答案和解析>>
科目: 来源: 题型:实验题
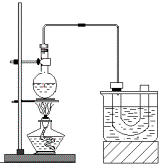 实验室制备溴乙烷(C2H5Br)的装置和步骤如图:(已知溴乙烷的沸点38.4℃)
实验室制备溴乙烷(C2H5Br)的装置和步骤如图:(已知溴乙烷的沸点38.4℃)查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| B. | 放热反应和吸热反应决定于反应物的总能量与生成物的总能量的相对大小 | |
| C. | 已知:S(s)+O2(g)=SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2;则△H1>△H2 | |
| D. | 凡经加热而发生的化学反应都是吸热反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验题
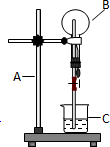 如图为氯化氢气体的喷泉实验装置.烧杯中的液体是紫色石蕊试液
如图为氯化氢气体的喷泉实验装置.烧杯中的液体是紫色石蕊试液查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{n(A-N+8)}{A+16}$ | B. | $\frac{n(A-N+10)}{(A+16)}$ | C. | A-N+2 | D. | $\frac{n(A-N+6)}{A}$ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 6.02×1023 就是阿佛加德罗常数 | |
| B. | 1 摩尔氢气含有2NA个氢原子 | |
| C. | 1 摩尔任何物质都含有6.02×1023 个分子 | |
| D. | 1 摩尔水含有18×6.02×1023 个分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com