
科目: 来源: 题型:选择题
| A. | S(g)<S(1)<S(s) | B. | S(g)>S(1)>S(s) | C. | S(g)>S(1)=S(s) | D. | S(g)>S(s)>S(1) |
查看答案和解析>>
科目: 来源: 题型:实验题
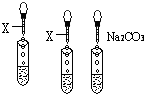 实验室有三瓶失去标签的无色溶液:氯化钾、氢氧化钙和稀硫酸,可用一种常见酸碱指示剂X 或Na2CO3一次鉴别它们.根据有关操作及所加试剂填空.
实验室有三瓶失去标签的无色溶液:氯化钾、氢氧化钙和稀硫酸,可用一种常见酸碱指示剂X 或Na2CO3一次鉴别它们.根据有关操作及所加试剂填空.查看答案和解析>>
科目: 来源: 题型:解答题
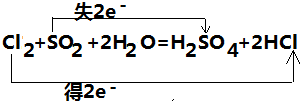
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | |
| B. | Na2O+H2O=2NaOH | |
| C. | Na2CO3+H2SO4=Na2SO4+CO2↑+H2O | |
| D. | MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O |
查看答案和解析>>
科目: 来源: 题型:实验题
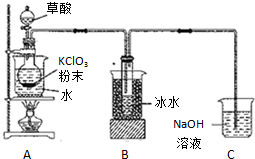 二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃.用KClO3粉末与草酸(H2C2O4)在60℃时反应可生成ClO2等物质,实验装置如图所示:
二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃.用KClO3粉末与草酸(H2C2O4)在60℃时反应可生成ClO2等物质,实验装置如图所示:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | C2H2 | B. | C2H5OH | C. | CH3CHO | D. | CH3COOH |
查看答案和解析>>
科目: 来源: 题型:选择题
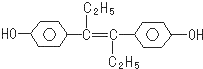
| A. | 己烯雌酚分子中碳原子的杂化轨道方式有sp2和sp3两种 | |
| B. | 己烯雌酚分子中所有的原子都可能在一个平面内 | |
| C. | 1mol己烯雌酚分子与溴水完全反应时,最多可消耗5molBr2 | |
| D. | 1mol己烯雌酚分子与氢气在一定条件下完全反应时,最多可消耗7molH2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 少量CuSO4(s) | B. | 2mol/L的硝酸溶液 | ||
| C. | 少量铜粉 | D. | 少量CH3COONa(s) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com