
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 若n(Cu2+):n(IO3-)=1:1,则每生成1molCuI转移6mol电子 | |
| B. | 若n(Cu2+):n(IO3-)=1:2,则每生成1molCuI转移12mol电子 | |
| C. | CuI既是氧化产物又是还原产物 | |
| D. | HI只有还原性没有氧化性 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Al3+ Mg2+ I- SO32- | B. | Mg2+ Na+ CO32- I- | ||
| C. | Al3+Na+ SO32- I- | D. | Na+ CO32- Br-I- |
查看答案和解析>>
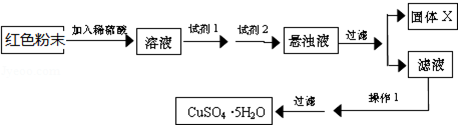
科目: 来源: 题型:解答题
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 室温下,1L0.3mol•L-1CH3COOH溶液和3L0.1 mol•L-1CH3COOH溶液中的H+数 | |
| B. | 纯水在25℃和80℃时的pH | |
| C. | 在NH3+NO→N2+H2O反应中,被氧化和被还原的N原子数 | |
| D. | 相同条件下,H2分别与Cl2、F2反应的反应速率 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 反应前酸、碱溶液的温度要相同 | |
| B. | 环形玻璃棒搅拌能加快反应速率,减小实验误差 | |
| C. | 为了使反应均匀进行,可以向酸(碱)中分次加入碱(酸) | |
| D. | 为了使反应更完全,可以使酸或碱适当过量 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
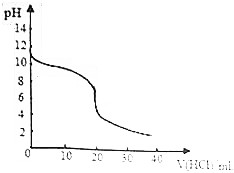 常温下,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的盐酸,pH随盐酸体积的变化如图所示.下列说法正确的是( )
常温下,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的盐酸,pH随盐酸体积的变化如图所示.下列说法正确的是( )| A. | 滴加盐酸10mL 时,c(Cl-)>c(NH4+)>c(NH3•H2O)>c(OH-)>c(H+) | |
| B. | 滴加盐酸20m时,c(H+)=c(OH-)+c(NH3•H2O) | |
| C. | 滴加盐酸10 mL时溶液的导电能力与滴加盐酸20mL时溶液的导电能力相同 | |
| D. | pH<7时,消耗盐酸的体积一定大于20.00mL |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 25℃时,1.0LpH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| B. | 1Llmol/LCH3COONa溶液中含有CH3COO-的数目为NA | |
| C. | agC2H4和C3H6的混合物中,所含原子的总数为3a$\frac{{N}_{A}}{14}$ | |
| D. | 常温常压下,0.1molCl2溶于水,转移的电子数目为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com