
科目: 来源: 题型:推断题
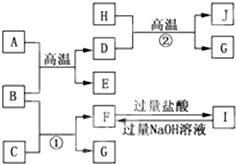 如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体.
如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
| ② | Cl2、FeBr2 | FeCl3、Br2 |
| ③ | MnO2… | Cl2、Mn2+… |
| A. | 第①组反应的其余产物为H2O | |
| B. | 第③组反应中生成1mol Cl2,转移电子4mol | |
| C. | 氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2 | |
| D. | 第②组反应中Cl2与 FeBr2的物质的量之比为3:2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ②④ | B. | ①③⑤ | C. | ①⑤⑥ | D. | ①④⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
 T℃时,将6mol CO2和8mol H2充入2L密闭恒容容器中,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化.下列说法正确的是( )
T℃时,将6mol CO2和8mol H2充入2L密闭恒容容器中,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化.下列说法正确的是( )| A. | 反应开始至a点时v(H2)=2 mol/(L•min) | |
| B. | 若曲线Ⅰ对应的条件改变是升温,则该反应放热反应 | |
| C. | 曲线Ⅱ对应的条件改变是降低压强 | |
| D. | 曲线Ⅱ对应的条件改变是加入催化剂 |
查看答案和解析>>
科目: 来源: 题型:选择题
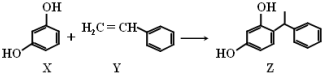
| A. | X、Y和Z均能使溴水褪色 | |
| B. | X和Z均能与Na2CO3溶液反应 | |
| C. | Y分子中所有原子可能在同一平面上 | |
| D. | Z能发生加成反应、取代反应,但不能发生氧化反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 一小块钠投入水中:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 用氢氧化钠溶液吸收过量二氧化碳 OH-+CO2═HCO3- | |
| D. | Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 写成2aA+2bB?2cC,Q值、K值均扩大了一倍 | |
| B. | 写成2aA+2bB?2cC,Q值扩大了一倍,K值保持不变 | |
| C. | 写成cC?aA+bB,Q值、K值变为原来的相反数 | |
| D. | 写成cC?aA+bB,Q值变为原来的相反数,K值变为倒数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com