
科目: 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 1:4 | D. | 1:5 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 成分 | 糖类 | 蛋白质 | 油脂 | 水 | 维生素 | 钙 | 铁 | 锌 |
| 质量/g | 0 | 16.6 | 5.2 | 78.2 | 0.00004 | 0.038 | 0.0008 | 0.0009 |
| A. | 六大类 | B. | 五大类 | C. | 四大娄 | D. | 三大类 |
查看答案和解析>>
科目: 来源: 题型:填空题
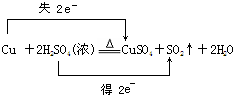 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na+、NO3-、Al3+、K+ | B. | Na+、ClO3-、ClO-、ClO4- | ||
| C. | K+、Cr2O72-、I-、Na+ | D. | Na+、SO32-、SO42-、NH4+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在氯化铝溶液中滴加氨水 | B. | 在偏铝酸钠溶液中通入CO2 | ||
| C. | 在氯化铝溶液中滴加氢氧化钠溶液 | D. | 在硫酸铝溶液中滴加偏铝酸钠溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分离碘单质和四氯化碳的混合物需要烧杯、玻璃棒和漏斗 | |
| B. | 用湿润的pH试纸测定溶液的pH一定会产生误差 | |
| C. | 实验室可以向浓硫酸中滴加浓盐酸制取少量氯化氢 | |
| D. | 用浓氨水可以除去试管内壁银镜 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | d | B. | 2d | C. | 3d | D. | 4d |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ③⑤ | B. | ②③ | C. | 只有③ | D. | ①④ |
查看答案和解析>>
科目: 来源: 题型:解答题
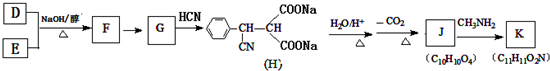
 ,则 D 的核磁共振氢谱有6种峰.F 中的无氧官能团为碳碳双键.
,则 D 的核磁共振氢谱有6种峰.F 中的无氧官能团为碳碳双键.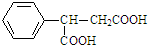 +CH3NH2$\stackrel{一定条件下}{→}$
+CH3NH2$\stackrel{一定条件下}{→}$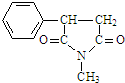 +2H2O.
+2H2O.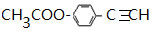 .
.查看答案和解析>>
科目: 来源: 题型:解答题
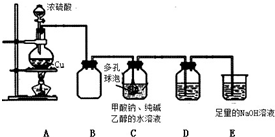
| 假 设 | 操作 | 现 象 | 原理 |
| Na2S2O4 为强 碱弱酸盐,其溶 液为碱性. | 取少量溶液于试管中,滴加 紫色石蕊试液 | 溶液变 成蓝色 | S2O42-水解,使溶液成碱性 |
| Na2S2O4 中 S 为 +3 价,具有较强 的还原性. | 取少量溶液于试管中,滴加过量新制氯水,再 滴加 BaCl2 溶液 | 有白色沉淀生 成 | 该反应的离子方程式依次为: 4H2O+S2O42-+3Cl2=2SO42-+6Cl-+8H+ Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com