
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 生活垃圾焚烧处理后体积一般可减少40%~50% | |
| B. | 生活垃圾焚烧处理后体积一般可减少80%~90% | |
| C. | 因为是封闭式焚烧处理所以没有烟气排放 | |
| D. | 发出的电也有污染,不能用作生活用电 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 全球气候变暖可能是由于二氧化碳含量的急剧增加 | |
| B. | 酸雨可以分为硫酸型酸雨和硝酸型酸雨 | |
| C. | 居室中的装潢材料缓慢释放出来的污染物中最常见的是甲醛、苯等有机物蒸气 | |
| D. | 检验居室中甲醛气体是否存在,可以抽取并通过品红溶液来检验 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 空气质量等级为优 | |
| B. | 二氧化硫的污染指数可能为42 | |
| C. | 目前,我国大部分地区空气中二氧化硫、二氧化氮及可吸入颗粒物等物质的含量偏高 | |
| D. | 对煤、石油等燃料进行脱硫处理、使用氢气等清洁燃料、通过静电沉降器除去悬浮颗粒物都可以治理大气污染,改善空气质量 |
查看答案和解析>>
科目: 来源: 题型:解答题

 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 为推广氢能的使用,工业上可采用电解水法制取大量氢气 | |
| B. | 将石油裂化、裂解,综合利用石油资源 | |
| C. | 有节制地开采煤、石油、天然气等矿物资源 | |
| D. | 将某些废旧塑料熔化后再成型 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. |  在新型催化剂作用下利用太阳能使水分解的能量变化曲线 | |
| B. |  KNO3溶解度曲线,α点所示溶液为50℃时的不饱和溶液 | |
| C. |  常温下pH=2的HCl溶液加水稀释倍数与pH的变化关系 | |
| D. |  10ml 0.01ml/L KMnO4酸性溶液与过量的0.1mol/L H2C2O4溶液混合时,n(Mn2+)随时间的变化(Mn2+对该反应有催化作用) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 阳离子只有氧化性,阴离子只有还原性 | |
| B. | 含氧酸可作氧化剂而无氧酸则不能 | |
| C. | 金属原子失电子数越多,其还原性越强 | |
| D. | 金属单质在反应中只作还原剂 |
查看答案和解析>>
科目: 来源: 题型:解答题
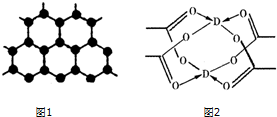 原子序数依次增大的四种主族元素A、B、C、D分别处于第一至第四周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体型分子,D原子外围电子排布为3d104s1.请回答下列问题:
原子序数依次增大的四种主族元素A、B、C、D分别处于第一至第四周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体型分子,D原子外围电子排布为3d104s1.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:推断题
 ;AB2的结构式是O=C=O.
;AB2的结构式是O=C=O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com