
科目: 来源: 题型:选择题
| A. | 在常温、常压下,11.2 L N2含有的分子数为0.5NA | |
| B. | 标准状况下,22.4 L H2和O2的混合气体所含分子数为NA | |
| C. | 在标准状况下,1 mol H2和1 mol H2O所占的体积都约为22.4 L | |
| D. | 标准状况下,1 mol CCl4的体积是22.4 L |
查看答案和解析>>
科目: 来源: 题型:选择题
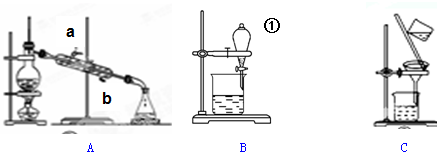
| A. | 实验必须使用温度计,且温度计的水银球应在蒸馏烧瓶的支管口处 | |
| B. | 冷凝管中的水流方向是从下口进入,上口排出 | |
| C. | 实验中需要在蒸馏烧瓶中加入几片碎瓷片,防止出现暴沸现象 | |
| D. | 用酒精灯加热时,蒸馏烧瓶必须垫石棉网 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温常压下,23gNO2与N2O4的混合物中含有NA个氧原子 | |
| B. | 一定条件下,1.4g N2和0.2mol H2混合充分反应,转移的电子数为0.3NA | |
| C. | 标准状况下,40g三氧化硫体积约为11.2L | |
| D. | 1L1mol•L?1的Na2CO3 溶液中阴离子数目小于NA |
查看答案和解析>>
科目: 来源: 题型:解答题
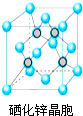 硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物.
硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物.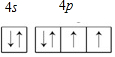 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在加热搅拌条件下加入MgO,可除去MgCl2溶液中的Fe3+ | |
| B. | 40mLlmol/LCH3COONa溶液与20mLlmol/LHCl溶液混合后溶液呈酸性,所得溶液中:c (CH3COO-)>c(Cl-)>c(H+)>c(OH-) | |
| C. | 常温下,Cd(OH)2和Co(OH)2的混合悬浊液中,c(Cd2+)是c(Co2+)的3.5倍 己知:Ksp[Cd(0H)2]=7.2×10-15,Ksp[Co(0H)2]=1.8×10-15 | |
| D. | 常温下,CH3COONa和CH3COOH的混合溶液中(pH=7):c(Na+)=c(CH3COO-)>c(H+)=c(OH-) |
查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2 L | |
| B. | 25℃,1.01×105 Pa,32 g O2和O3的混合气体所含原子数为2.5NA | |
| C. | 标准状况下,11.2 L H2O含有的原子数为1.5NA | |
| D. | 常温常压下,44 g CO2含有的原子数为3NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 离子的还原性强弱:I->Fe2+>Br- | |
| B. | 当a≥b时,发生的离子反应:2I-+Br2═I2+2Br- | |
| C. | 当5a=4b时,反应后的离子浓度之比:c(Fe2+):c(Fe3+):c(Br-)=1:1:5 | |
| D. | 当3a≤2b时,发生的离子反应:2Fe2++2I-+2Br2═2Fe3++I2+4Br- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HCl、NaCl溶于水,破坏的化学键类型相同 | |
| B. | 某物质中含有离子键,则该物质在任何条件下均可导电 | |
| C. | 干冰是分子晶体,其气化过程中只需克服分子间作用力 | |
| D. | 常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com