
科目: 来源: 题型:选择题
| 实验事实 | 结论 | |
| ① | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| ② | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| ③ | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| ④ | 常温下白磷可自燃而氮气需在放电时才与氧气反应 | 非金属性:P>N |
| ⑤ | 某无色晶体加入氢氧化钠浓溶液中并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该晶体中一定有NH4+ |
| A. | ②③⑤ | B. | ①②③ | C. | ③④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目: 来源: 题型:实验题
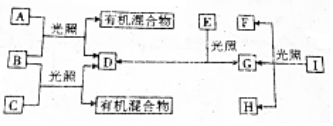
 ,有机物C的结构简式为
,有机物C的结构简式为 ,其苯环上的二氯代物共有6种.
,其苯环上的二氯代物共有6种.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
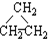
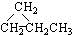
| A. | ⑤和⑥ | B. | ①和③ | C. | ①和④ | D. | ①和② |
查看答案和解析>>
科目: 来源: 题型:解答题
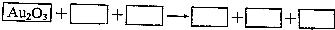

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将可调高度的铜丝伸入稀硝酸中,溶液变蓝,说明Cu与稀硝酸发生置换反应 | |
| B. | 稀硝酸可除去试管内壁的银镜 | |
| C. | 常温下,将浓硝酸滴加到用砂纸打磨过上,会产生红棕色气体 | |
| D. | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液,则会有气体生成,溶液呈红色,说明稀硝酸将Fe氧化为Fe3+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径大小:Z>Y>X>W | |
| B. | 由W元素形成的单质一定是原子晶体,其熔沸点很高 | |
| C. | W、Y、Z三种元素形成的气态氢化物中最稳定的是Z的气态氢化物 | |
| D. | Y、Z所形成的氧化物的水化物的酸性为:Y<Z |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe2+ | B. | Fe3+ | C. | Al3+ | D. | NH4+ |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验题
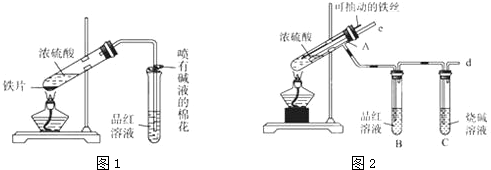
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com