
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| ±ąŗÅ | 0.1mol/L H2C2O4 ČÜŅŗµÄĢå»ż/mL | 0.01mol/L ĖįŠŌ KMnO4 µÄĢå»ż/mL | ÕōĮóĖ®µÄĢå»ż/mL | ĪĀ¶Č/”ę |
| ¢Ł | 2 | 4 | 2 | 25 |
| ¢Ś | 3 | |||
| ¢Ū | 50 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
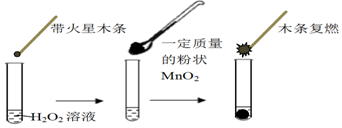
| MnO2µÄÖŹĮæ/g | 0.1 | 0.2 | 0.4 |
| 40sÄ©O2Ģå»ż/mL | 49 | 61 | 86 |
| ŹŌ¹Ü | ¢ń | ¢ņ | ¢ó |
| µĪ¼ÓŹŌ¼Į | 5µĪ0.1mol•L-1FeCl3 | 5µĪ0.1mol•L-1 CuCl2 | 5µĪ0.3mol•L-1 NaCl |
| ²śÉśĘų ÅŻĒéæö | ½Ļæģ²śÉśĻøŠ”ĘųÅŻ | »ŗĀż²śÉśĻøŠ”ĘųÅŻ | ĪŽĘųÅŻ²śÉś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
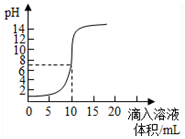
| A£® | ŌĄ“ŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ0.1mol•L-1 | |
| B£® | æÉŅŌŃ”ŌńŗģÉ«ŹÆČļ×÷ĪŖÖøŹ¾¼Į | |
| C£® | ĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæÅضČĪŖ0.1mol•L-1 | |
| D£® | pHĪŖ7Ź±¼ÓČėµÄĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæĪŖ0.1mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | cµć¶ŌÓ¦µÄČÜŅŗÖŠ“óĮæ“ęŌŚµÄĄė×ÓæÉÄÜĪŖ£ŗNa+”¢H+”¢Cl-”¢NO3- | |
| B£® | ½«25”ꏱµÄKClČÜŅŗ¼ÓČȵ½t”ę£¬ŌņøĆČÜŅŗÖŠµÄc£ØOH-£©ÓÉaµć±ä»Æµ½bµć | |
| C£® | t”ę£¼25”ę | |
| D£® | acĻßÉĻµÄČĪŅāŅ»µćČÜŅŗ¾łÓŠc£ØH+£©=c£ØOH-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪŖ·ĄÖ¹ĢśÉśŠā£¬ŌŚĘä±ķĆęĶæŅ»²ć·ĄŠāÓĶĘį | |
| B£® | ĪŖ·ĄÖ¹»šŌÖ£¬ŌŚĆę·Ū³§”¢¼ÓÓĶÕ¾µČ³”ĖłŅŖŃĻ½ūŃĢ»š | |
| C£® | ĪŖ¼ÓæģKClO3µÄ·Ö½āĖŁĀŹ£¬¼ÓČėMnO2 | |
| D£® | ĪŖĢįøßH2O2µÄ·Ö½āĀŹ£¬ĻņČÜŅŗÖŠµĪ¼ÓFeCl3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
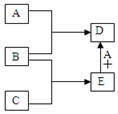 ŅŃÖŖA”¢B”¢C”¢D”¢E¾łĪŖ֊ѧ»Æѧ֊³£¼ūĪļÖŹ£¬ŌŚŅ»¶ØĢõ¼žĻĀĻą»„×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø·“Ó¦Ģõ¼žŗĶ²æ·Ö²śĪļŅŃŹ”ĀŌ£©£®
ŅŃÖŖA”¢B”¢C”¢D”¢E¾łĪŖ֊ѧ»Æѧ֊³£¼ūĪļÖŹ£¬ŌŚŅ»¶ØĢõ¼žĻĀĻą»„×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø·“Ó¦Ģõ¼žŗĶ²æ·Ö²śĪļŅŃŹ”ĀŌ£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1ÖÖ | B£® | 2ÖÖ | C£® | 3ÖÖ | D£® | 4ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³ĪĒåŹÆ»ŅĖ®ÓėÉŁĮæĖÕ“ņČÜŅŗ»ģŗĻ£ŗCa2++OH-+HCO3-ØTCaCO3”ż+H2O | |
| B£® | ¹żŃõ»ÆÄĘČÜÓŚĖ®£ŗ2022-+2H2OØT4OH-+O2”ü | |
| C£® | ½«¹żĮ涞Ńõ»ÆĮņĘųĢåĶØČė°±Ė®ÖŠ£ŗSO2+NH3•H2OØTHSO3-+NH4+ | |
| D£® | ĻņBa£ØOH£©2ČÜŅŗÖŠµĪ¼ÓĻ”ĮņĖį£ŗBa2++OH-+H++SO42-ØTBaSO4”ż+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĮņĖį”¢“æ¼ī”¢“×ĖįÄĘŗĶÉśŹÆ»Ņ·Ö±šŹōÓŚĖį”¢¼ī”¢ŃĪŗĶŃõ»ÆĪļ | |
| B£® | ČÕ³£Éś»īÖŠĪŽĖ®ŅŅ“¼³£ÓĆӌɱ¾śĻū¶¾ | |
| C£® | SO2¾ßÓŠĘư׊Ō£¬ÄÜŹ¹µāµÄµķ·ŪČÜŅŗÓÉĄ¶É«±äĪŖĪŽÉ« | |
| D£® | ÕįĢĒ”¢ĮņĖį±µŗĶĖ®·Ö±šŹōÓŚ·Ēµē½āÖŹ”¢Ēæµē½āÖŹŗĶČõµē½āÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ČēĶ¼ŹĒŅ»øö»Æѧ¹ż³ĢµÄŹ¾ŅāĶ¼£®Ēėøł¾ŻøĆŹ¾ŅāĶ¼Ķź³ÉĻĀĮŠĢāÄæ£ŗ
ČēĶ¼ŹĒŅ»øö»Æѧ¹ż³ĢµÄŹ¾ŅāĶ¼£®Ēėøł¾ŻøĆŹ¾ŅāĶ¼Ķź³ÉĻĀĮŠĢāÄæ£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com