
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| µĪ¶Ø“ĪŹż | “ż²āŅŗĢå»ż/ml | ±ź×¼ŃĪĖįĢå»ż/ml | |
| µĪ¶ØĒ°¶ĮŹż/ml | µĪ¶Øŗó¶ĮŹż/ml | ||
| µŚŅ»“Ī | 10.00 | 0.20 | 22.90 |
| µŚ¶ž“Ī | 10.00 | 0.50 | 20.40 |
| µŚČż“Ī | 10.00 | 4.00 | 24.10 |
| µŚĖÄ“Ī | 10.00 | 0.00 | 20.00 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
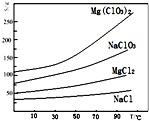 ĀČĖįĆ¾[Mg£ØClO3£©2]³£ÓĆ×÷“ߏģ¼Į”¢³ż²Ż¼ĮµČ£¬ŹµŃéŹŅÓĆĀ±æé£ØÖ÷ŅŖ³É·ÖĪŖMgCl2•6H2O£¬ŗ¬ÓŠMgSO4”¢FeCl2µČŌÓÖŹ£©ÖʱøÉŁĮæMg£ØClO3£©2•6H2OµÄĮ÷³ĢČēĻĀ£ŗ
ĀČĖįĆ¾[Mg£ØClO3£©2]³£ÓĆ×÷“ߏģ¼Į”¢³ż²Ż¼ĮµČ£¬ŹµŃéŹŅÓĆĀ±æé£ØÖ÷ŅŖ³É·ÖĪŖMgCl2•6H2O£¬ŗ¬ÓŠMgSO4”¢FeCl2µČŌÓÖŹ£©ÖʱøÉŁĮæMg£ØClO3£©2•6H2OµÄĮ÷³ĢČēĻĀ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| ÄŃČܵē½āÖŹ | Mg£ØOH£©2 | Cu£ØOH£©2 | Fe£ØOH£©2 | Fe£ØOH£©3 |
| Čܽā¶Č/g | 9”Į10-4 | 1.7”Į10-6 | 1.5”Į10-4 | 3.0”Į10-9 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉżøßĪĀ¶Č£¬¹ĢĢåµÄĮæ¼õÉŁ | |
| B£® | ¼ÓČėÉŁĮæNa2CO3·ŪÄ©ÄÜŌö“óøĘĄė×ÓµÄÅØ¶Č | |
| C£® | ½µµĶĪĀ¶Č£¬ČÜŅŗÖŠc£ØOH-£©Ōö“ó | |
| D£® | ŗćĪĀĻĀ¼ÓČėÉŁĮæCaO£¬ČÜŅŗµÄpHŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼ÓMgSO4 | B£® | ¼ÓHClČÜŅŗ | C£® | ¼ÓNaOH | D£® | ¼ÓÉŁĮæĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | AgCl²»ČÜÓŚĖ®£¬²»ÄÜ×Ŗ»ÆĪŖAgI | |
| B£® | ŌŚŗ¬ÓŠÅØ¶Č¾łĪŖ0.001 mol•L-1µÄCl-”¢I-µÄČÜŅŗÖŠ»ŗĀż¼ÓČėAgNO3Ļ”ČÜŅŗ£¬Ź×ĻČĪö³öAgI³Įµķ | |
| C£® | AgI±ČAgCløüÄŃČÜÓŚĖ®£¬ĖłŅŌ£¬AgClæÉŅŌ×Ŗ»ÆĪŖAgI | |
| D£® | ³£ĪĀĻĀ£¬AgClČōŅŖŌŚNaIČÜŅŗÖŠæŖŹ¼×Ŗ»ÆĪŖAgI£¬ŌņNaIµÄÅØ¶Č±ŲŠė²»µĶÓŚ$\frac{1}{\sqrt{1.8}}$”Į10-11mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
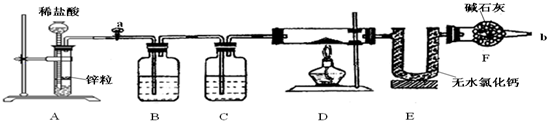
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĪļÖŹ | Cu£ØOH£©2 | Fe£ØOH£©3 | CuCl | CuI |
| Ksp | 2.2”Į10-20 | 2.6”Į10-39 | 1.7”Į10-7 | 1.3”Į10-12 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±äĪŖŌĄ“µÄ10-3±¶ | B£® | ±äĪŖ ŌĄ“µÄ10-2±¶ | ||
| C£® | ±äĪŖŌĄ“µÄ103±¶ | D£® | ²»·¢Éś±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ö»ÓŠAgCl ³Įµķ | B£® | Ö»ÓŠAgI ³Įµķ | ||
| C£® | AgCl”¢AgI ¶¼³Įµķ£¬ŅŌAgCl ĪŖÖ÷ | D£® | AgCl”¢AgI ¶¼³Įµķ£¬ŅŌAgI ĪŖÖ÷ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com