
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
48 20 |
249 97 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

| 气体 | CH3OCH3 | H2O | N2 | A |
| 体积(m3) | 95 | 95 | x | y |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 催化剂 |
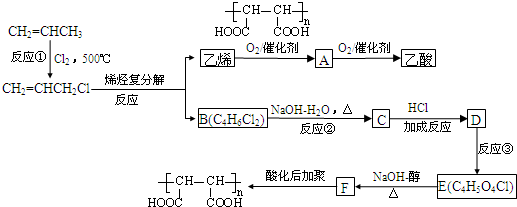
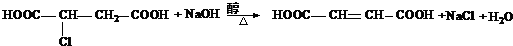
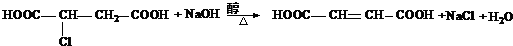
查看答案和解析>>
科目: 来源: 题型:
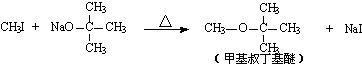
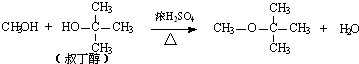
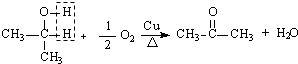 试推测叔丁醇是否能发生类似反应
试推测叔丁醇是否能发生类似反应

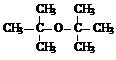
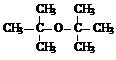
查看答案和解析>>
科目: 来源: 题型:阅读理解
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
| 温度/℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4?7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |
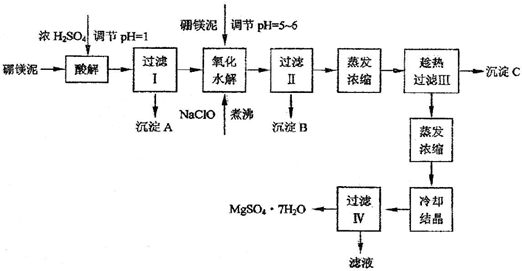
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com