
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 ;Y的价电子轨道表示式为
;Y的价电子轨道表示式为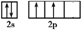 .
.查看答案和解析>>
科目: 来源: 题型:实验题

查看答案和解析>>
科目: 来源: 题型:解答题
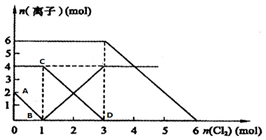 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该溶液中可能含K+ | |
| B. | 该溶液中肯定含有NO3-、SO42-、NH4+、CO32- | |
| C. | 该溶液中一定不含NO3- | |
| D. | 该溶液中一定含K+,且c(K+)≥0.1mol/L |
查看答案和解析>>
科目: 来源: 题型:实验题

| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水和酒精 |
| B | 17.9 | 290 | 1.26 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 小苏打溶液中加入NaOH溶液:H ++OH-=H2O | |
| B. | 氧化铁与稀盐酸反应:FeO+2H+=Fe2++H2O | |
| C. | 硫酸铜溶液与氢氧化钡溶液混合:Cu2++2OH-=Cu(OH)2↓ | |
| D. | 氯化钡与纯碱溶液反应:Ba2++CO32-=BaCO3↓ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | C(s)+H2O(g)=CO(g)+H2(g)△H>0 | B. | NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1)△H<0 | ||
| C. | 2CO(g)+O2(g)=2CO2(1)△H<0 | D. | 2H2(g)+O2(g)═2H2O(l)△H<0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com