
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2ŌŚCl2ÖŠČ¼ÉÕ | B£® | Ėį¼īÖŠŗĶ·“Ó¦ | ||
| C£® | ŅŗĢ¬Ė®±ä³ÉĖ®ÕōĘų | D£® | ÅØĮņĖįĻ”ŹĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŠčŅŖ¼ÓČČ²ÅÄÜ·¢ÉśµÄ·“Ó¦Ņ»¶ØŹĒĪüČČ·“Ó¦ | |
| B£® | »Æѧ±ä»Æ¹ż³ĢŹĒŌ×ÓµÄÖŲŠĀ×éŗĻ¹ż³Ģ | |
| C£® | Éś³ÉĪļ×ÜÄÜĮæøßÓŚ·“Ó¦Īļ×ÜÄÜĮæµÄ·“Ó¦ŹĒĪüČČ·“Ó¦ | |
| D£® | ·“Ó¦ŹĒ·ÅČČ»¹ŹĒĪüČȱŲŠėæ“·“Ó¦ĪļŗĶÉś³ÉĪļĖł¾ßÓŠµÄ×ÜÄÜĮæµÄĻą¶Ō“óŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
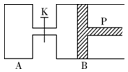 Ķ¼ÖŠ£¬PĪŖŅ»æÉ×ŌÓÉ»¬¶ÆµÄ»īČū£¬¹Ų±ÕK£¬·Ö±šĻņČŻĘ÷A”¢BÖŠø÷³äČė1mol X”¢1mol Y£¬ĘšŹ¼Ź±£¬VA=a L£¬VB=0.8a L£ØĮ¬ĶعܵÄĢå»żŗöĀŌ²»¼Ę£©£¬ŌŚĻąĶ¬ĪĀ¶ČŗĶÓŠ“߻ƼĮ“ęŌŚµÄĢõ¼žĻĀ£¬Į½ČŻĘ÷ÖŠø÷×Ō·¢ÉśĻĀŹö·“Ó¦£ŗ3X£Øg£©+3Y£Øg£©?2Z£Øg£©+2W£Øg£©£¬“ļĘ½ŗāŹ±£¬VB=0.6a L£®»Ų“šĻĀĮŠĪŹĢā£ŗ
Ķ¼ÖŠ£¬PĪŖŅ»æÉ×ŌÓÉ»¬¶ÆµÄ»īČū£¬¹Ų±ÕK£¬·Ö±šĻņČŻĘ÷A”¢BÖŠø÷³äČė1mol X”¢1mol Y£¬ĘšŹ¼Ź±£¬VA=a L£¬VB=0.8a L£ØĮ¬ĶعܵÄĢå»żŗöĀŌ²»¼Ę£©£¬ŌŚĻąĶ¬ĪĀ¶ČŗĶÓŠ“߻ƼĮ“ęŌŚµÄĢõ¼žĻĀ£¬Į½ČŻĘ÷ÖŠø÷×Ō·¢ÉśĻĀŹö·“Ó¦£ŗ3X£Øg£©+3Y£Øg£©?2Z£Øg£©+2W£Øg£©£¬“ļĘ½ŗāŹ±£¬VB=0.6a L£®»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

| ŅŅ“¼ | 1£¬2¶žäåŅŅĶé | ŅŅĆŃ | |
| דĢ¬ | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå |
| ĆܶČ/g•cm-3 | 0.79 | 2.2 | 0.71 |
| ·Šµć/”ę | 78.5 | 132 | 34.6 |
| ČŪµć/”ę | -130 | 9 | -116 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 4ÖÖ | B£® | 6ÖÖ | C£® | 8ÖÖ | D£® | 10ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
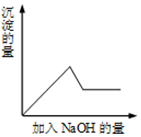 ÓŠŅ»ĪŽÉ«ČÜŅŗ£¬ĘäÖŠæÉÄÜŗ¬ÓŠFe3+”¢Cu2+”¢K+”¢Al3+”¢Mg2+”¢SO42-”¢Cl-µČĄė×ÓÖŠµÄ¼øÖÖ£¬ĪŖ·ÖĪöĘä³É·Ö£¬Č”“ĖČÜŅŗ·Ö±š½ųŠŠĮĖČżøöŹµŃ飬Ęä²Ł×÷ŗĶÓŠ¹ŲĻÖĻóČēĻĀ£ŗ
ÓŠŅ»ĪŽÉ«ČÜŅŗ£¬ĘäÖŠæÉÄÜŗ¬ÓŠFe3+”¢Cu2+”¢K+”¢Al3+”¢Mg2+”¢SO42-”¢Cl-µČĄė×ÓÖŠµÄ¼øÖÖ£¬ĪŖ·ÖĪöĘä³É·Ö£¬Č”“ĖČÜŅŗ·Ö±š½ųŠŠĮĖČżøöŹµŃ飬Ęä²Ł×÷ŗĶÓŠ¹ŲĻÖĻóČēĻĀ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
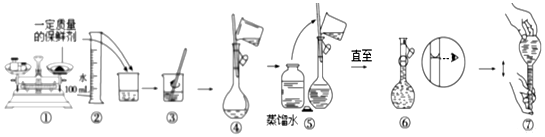
| ³É·Ö | ÖŹĮæ£Øg£© | Ħ¶ūÖŹĮæ£Øg•mol-1£© |
| ÕįĢĒ | 25.00 | 342 |
| ĮņĖį¼Ų | 0.87 | 174 |
| °¢Ė¾Ę„ĮÖ | 0.17 | 180 |
| øßĆĢĖį¼Ų | 0.316 | 158 |
| ĻõĖįŅų | 0.075 | 170 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SiO2ŹĒÓɼ«ŠŌ¼ü¹¹³ÉµÄ·Ē¼«ŠŌ·Ö×Ó | |
| B£® | ČōNA±ķŹ¾°¢·üŁ¤µĀĀŽ³£Źż£¬³£ĪĀ³£Ń¹ĻĀ60g SiO2ÖŠŗ¬ÓŠµÄ¹²¼Ū¼üŹżÄæĪŖ2NA | |
| C£® | Ģ¼ŗĶ¹čĶ¬Ö÷×壬Ņņ“ĖCO2ŗĶSiO2»ÆѧŠŌÖŹĻąĖĘ£¬ĪļĄķŠŌÖŹŅ²ĻąĖĘ | |
| D£® | SiO2¾§Ģå½į¹¹ÖŠµÄ×īŠ”»·ĪŖ6øöSiŗĶ6øöO×é³ÉµÄ12ŌŖ»· |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com