
科目: 来源: 题型:选择题
| A. | Fe3+、Na+、Cl-、OH- | B. | Fe3+、Cl-、K+、Ca2+ | ||
| C. | Cl-、Ca2+、Mg2+、CO32- | D. | Ba2+、K+、CO32-、Cl- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.1mol的NaHSO4溶液中含0.2NA个阳离子 | |
| B. | 1L0.1mol/L的乙醇溶液中所含的分子总数为0.1NA个 | |
| C. | 在标准状况下,含NA个氦原子(He)的氦气所含的分子数是0.5NA个 | |
| D. | 1mol FeCl3跟沸水完全反应转化为氢氧化铁胶体,其中胶粒的数目一定少于NA个 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,1L 0.1mol/L HCl溶液中含氢原子数是0.1NA | |
| B. | 标准状况下,2.24L由CO2和O2组成的混合气体中含氧分子数是0.1NA | |
| C. | 10g碳酸钙与足量的稀盐酸充分反应消耗的氢离子数为0.1NA | |
| D. | 标准状况下,11.2L CO和 NO混合气体中与11.2LN2中分子数均为0.5NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 由W 与X 组成的化合物的沸点总低于由W与Y组成的化合物的沸点 | |
| B. | 以上四种元素的原子半径大小为W<X<Y<Z | |
| C. | Y的气态简单氢化物的稳定性比Z的强 | |
| D. | W、Y、Z三种元素可形成离子化合物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 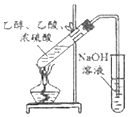 实验室中制取少量的乙酸乙酯 | B. | 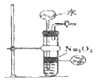 制备少量氧气 | ||
| C. |  验证NaHCO3和Na2CO3的热稳定性 | D. | 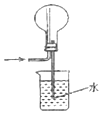 氯化氢气体的吸收 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氧化剂和还原剂物质的量之比为5:4 | |
| B. | 3 mol H2S可还原4mol的KIO3 | |
| C. | I2是还原产物,K2SO4是氧化产物 | |
| D. | 1molKIO3可氧化0.2mol的KI |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | c=1000Wρ/M | B. | m=VρW/100 | C. | W%=cM/1000ρ% | D. | c=100m/VM |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 金属镁与稀盐酸反应:有气体生成,Mg+2 H++2Cl-═MgCl2+H2↑ | |
| B. | 氯化钡溶液与硫酸反应:有白色沉淀生成:SO42-+Ba2+═BaSO4↓ | |
| C. | 碳酸钠溶液与盐酸反应:有气泡逸出:Na2CO3+2 H+═2Na++CO2↑+H2O | |
| D. | 过量铁粉与氯化铜溶液反应:溶液由蓝色变成浅绿色,同时有红色固体生成:Fe+Cu2+═Fe3++Cu |
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:实验题
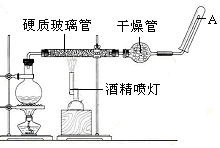 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com