
科目: 来源: 题型:解答题
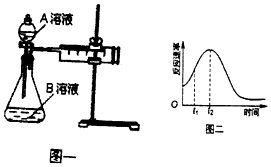
| 实验序号 | A溶液 | B溶液 |
| ① | 20 mL 0.1 mol•L-1H2C2O4溶液 | 30 mL 0.01 mol•L-1kMnO4溶液 |
| ② | 20 mL 0.2 mol•L-1 H2C2O4溶液 | 30 mL 0.01 mol•L-1KMnO4溶液 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| 弱酸化学式 | HF | HClO | H2CO3 |
| 电离平衡常数 | 6.8×10-9 | 4.7×10-15 | K1=4.4×10-7 K2=4.7×10-11 |
| A. | 常温下,同物质的量浓度的HF与H2CO3溶液,前者的c(H+)较小 | |
| B. | 若某溶液中c(F-)=c(ClO-),往该溶液中滴入HCl,F-比ClO-更易结合H+ | |
| C. | 往饱和Na2CO3溶液中逐滴加入稀盐酸至过量,所得溶液中c(HCO3-)先增大后减小 | |
| D. | 同温下,等体积、等c(H+)的HF和HClO分别与NaOH完全反应,消耗等量的NaOH |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 先配制一定量的0.10mol/LCH3COOH溶液,然后测溶液的c(H+),若c(H+)小于0.10mol/L,则可证明醋酸为弱电解质 | |
| B. | 先配制一定量0.0010mol•L-1和0.10mol•L-1的CH3COOH,分别用pH计测它们的c(H+),若前者的c(H+)与后者c(H+)的比值小于10,则可证明醋酸是弱电解质 | |
| C. | 取等体积、等c(H+)的CH3COOH溶液和盐酸分别于足量等规格的锌粒反应,若反应过程中醋酸产生H2较慢且最终产生H2较多,则可证明醋酸是弱电解质 | |
| D. | 取等体积、等c(H+)的CH3COOH溶液和盐酸分别加水稀释相同的倍数,若稀释后CH3COOH溶液中c(H+)大,则可证明醋酸是弱电解质 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 3C(s)+CaC(s)?CaC2 (s)+CO(g)在常温下不能自发进行,说明该反应的△H>0 | |
| B. | CH3COOH溶液加水稀释后,溶液中$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$的值增大 | |
| C. | 恒温恒压的密闭容器中进行反应:N2(g)+3H2(g)?2NH3(g)△H=-aKJ/mol,平衡时向容器中在充入一定量的NH3,重新达到平衡时a值不变 | |
| D. | C(s)+H2O(g)?CO(g)+H2(g) (△H>0),其它条件不变时,升高温度,正反应速率增大,逆反应速率减小,平衡正向移动 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 对由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色加深 | |
| B. | 使用铁作催化剂,使N2和H2在一定条件下合成为NH3 | |
| C. | 可用排饱和食盐水法收集氯气 | |
| D. | 500℃时比室温更有利于合成氨的反应(已知合成氨的反应时放热反应) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 影响化学反应速率的主要因素是内因,即反应物本身的性质 | |
| B. | 增大反应物浓度,活化分子百分数不变,单位体积内活化分子数增多 | |
| C. | 升高温度,活化分子百分数增大,分子有效碰撞的频率增大,化学反应速率加快 | |
| D. | 使用正催化剂,活化分子百分数不变,但是反应速率加快 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 高锰酸钾酸性溶液与草酸钾溶液反应:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O | |
| B. | KI的酸性溶液长期置于空气中::4I-+4H++O2═2I2+2H2O | |
| C. | 硫代硫酸钠溶液中滴加稀硫酸:2H++S2O32-═S↓+SO2↑+H2O | |
| D. | 用食醋除去水垢:CO32-+2CH3COOH═H2O+CO2↑+2CH3COO- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2CO3?2H++CO32- | B. | Ca(OH)2?Ca2++2OH- | ||
| C. | Fe2(SO4)3?2Fe2++3SO42- | D. | NaHCO3?Na++HCO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ④⑦ | B. | ⑦ | C. | ①②⑤⑦ | D. | ①③④⑥⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com