
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:推断题
 有A、B是钠的两种常见的化合物的混合物,其相互转化关系如图(其他略去)
有A、B是钠的两种常见的化合物的混合物,其相互转化关系如图(其他略去)查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:解答题

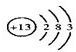 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,22.4L水中含有的分子数是NA个 | |
| B. | 32g氧气中含有的分子数为NA | |
| C. | 1mol氯气与足量的氢氧化钠溶液反应,转移的电子数为2NA | |
| D. | 1L1mol/LCaCl2溶液中含有的氯离子数为NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 漂白粉保存在烧杯中 | |
| B. | 氯水保存在无色透明的试剂瓶中 | |
| C. | 金属钠着火燃烧时用砂子灭火 | |
| D. | 大量氯气泄漏时用氢氧化钠溶液浸湿的软布蒙面并迅速离开现场 |
查看答案和解析>>
科目: 来源: 题型:解答题
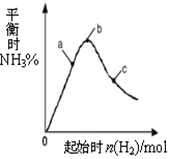 工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等.
工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等.查看答案和解析>>
科目: 来源: 题型:选择题
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
| A. | 五种物质在常温下溶解度最大的是Ag 2SO4 | |
| B. | 将AgCl溶解于水后,向其中加入Na2S,则可以生成黑色的Ag2S沉淀 | |
| C. | 沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动 | |
| D. | 常温下,AgCl、AgBr和AgI三种物质的溶解度逐渐增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com