
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:选择题
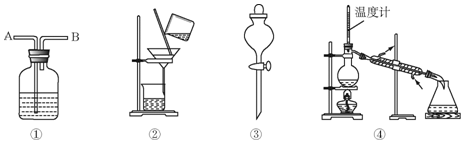
| 选项 | 物质 | 试剂 | 装置 |
| A | C2H6(C2H4) | ① | ① |
| B | 苯(苯酚) | ⑥ | ② |
| C | 苯(苯甲酸) | ⑤ | ④ |
| D | 甲苯(二甲苯) | ③ | ③ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:实验题
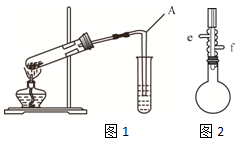 酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业,表格中给出了一些物质的物理常数,请回答下列问题
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业,表格中给出了一些物质的物理常数,请回答下列问题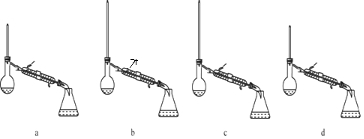
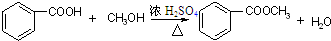 .
.查看答案和解析>>
科目: 来源: 题型:解答题
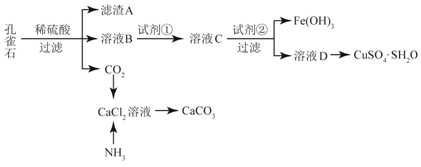
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | V(NaOH)=0时,c(H+)=1×10-2mol•L-1 | |
| B. | V(NaOH)=10mL时,c(H+)=1×10-7mol•L-1 | |
| C. | V(NaOH)>10mL时,c(Na+)>c(C2O42-)>c(HC2O4-) | |
| D. | V(NaOH)<10mL时,不可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) |
查看答案和解析>>
科目: 来源: 题型:选择题
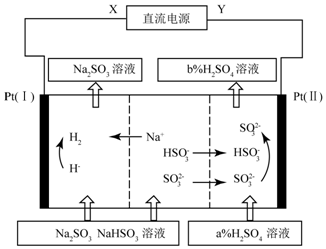
| A. | X为直流电源的正极,Y为直流电流的负极 | |
| B. | 图中的b<a | |
| C. | P(I)附近溶液的pH减小,Pt(II)附近溶液的pH增大 | |
| D. | 再生机理为:Pt(I)H+放电,导致“HSO3-?SO2-+H+”平衡右移 |
查看答案和解析>>
科目: 来源: 题型:选择题
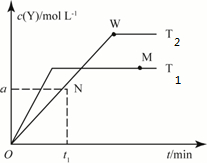 ( )
( )| A. | T2下,在0~t1时间内v(X)=$\frac{a}{{t}_{1}}$mol•L-1•min-1 | |
| B. | N点时气体的总压强大于W点时气体的总压强 | |
| C. | M点的正反应速率小于N点的逆反应速率 | |
| D. | W点时再加入一定量Y,平衡后X的转化率减小 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H+、Na+、OH-、SO42- | B. | Na+、Ca2+、CO32-、NO3- | ||
| C. | K+、H+、SO42-、Al3+ | D. | Na+、H+、Cl-、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com