
科目: 来源: 题型:选择题
| A. | 加热完毕后,用嘴吹灭酒精灯 | |
| B. | 过滤时,漏斗下端紧贴烧杯内壁 | |
| C. | 给烧杯加热时,不需要垫上石棉网 | |
| D. | 用托盘天平称量 NaOH 固体时,被称量的 NaOH 固体放在滤纸上 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 干冰可用于人工降雨 | |
| B. | 雷雨时空气中的 N2可变为氮的化合物 | |
| C. | 使用合适的催化剂可将水变成汽油 | |
| D. | 一定条件下石墨能变成金刚石 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 盛 FeSO4溶液的锥形瓶滴定前用 FeSO4溶液润洗 2-3 次 | |
| B. | 选碱式滴定管盛放标准 KMnO4溶液,并用碘化钾淀粉溶液作指示剂 | |
| C. | 滴定前仰视读数,滴定后俯视读数会导致滴定结果偏低 | |
| D. | 锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 充电时阴极区电解质溶液 pH 降低 | |
| B. | 在使用过程中此电池要不断补充水 | |
| C. | 放电时 NiOOH 在电极上发生氧化反应 | |
| D. | 充电时阳极反应为:Ni(OH)2-e-+OH-=NiOOH+H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
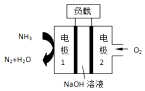
| A. | 电池总反应为:4NH3+3O2=2N2+6H2O | |
| B. | 电池工作时,OH-向正极移动 | |
| C. | 电极 2 发生的电极反应为:O2+4H++4e-=2H2O | |
| D. | 电流由电极 1 经外电路流向电极2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,某溶液中由水电离出来的 c(H+)=1×10-amol•L-1,若 a<7,则该溶液可能为 NaHSO4溶液 | |
| B. | 中和同体积、同 pH 的硫酸、盐酸和醋酸所需相同浓度的 NaOH 溶液的体积关系:V(硫酸)>V(盐酸)>V(醋酸) | |
| C. | 向 AgCl 悬浊液中加入 NaCl 固体,AgCl 沉淀的溶度积(Ksp)变小 | |
| D. | pH 相等的①CH3COONa ②NaHCO3溶液中,c(Na+)大小关系:②<① |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 过程中银器一直保持恒重 | |
| B. | 银器为正极,Ag2S 被还原生成单质银 | |
| C. | 铝质容器为正极 | |
| D. | 黑色褪去的原因是黑色 Ag2S 转化为白色 AgCl |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该溶液可能由等物质的量浓度等体积的 NaOH 溶液和 CH3COOH 溶液混合而成 | |
| B. | 该溶液可能由 pH=3 的 CH3COOH 与 pH=11 的 NaOH 溶液等体积混合而成 | |
| C. | 加入适量 NaOH,溶液中离子浓度为 c(CH3COO- )>c(Na+)>c(OH-)>c(H+) | |
| D. | 加入适量氨水,c(CH3COO-)一定大于 c(Na+)、c(NH4+)之和 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com