
科目: 来源: 题型:选择题
| A. | 干冰中分子的堆积方式为非密堆积 | |
| B. | 金属晶体中原子的最大配位数为12 | |
| C. | 晶体硅熔化时需破坏非极性共价键 | |
| D. | 冰融化为水的过程中其密度先变大,超过4℃后又逐渐变小 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,8.0gSO3体积为2.24L | |
| B. | 物质的量为1molSO2、CO2的混合物所含氧原子数为2NA | |
| C. | 0.1molFeCl3溶液中含有的Fe3+数为0.1NA | |
| D. | 0.5mol镁在空气中完全燃烧所需要的氧气的物质的量为0.25mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 16gO2和O3的混合物中O原子的电子数为8NA | |
| B. | 标准状况下,2.24L氯气与水反应,转移的电子数为0.1NA | |
| C. | 28g乙烯与丙烯混合物中含有C-H键的数目为4NA | |
| D. | 常温下,1LpH=11的Na2CO3溶液中由水电离出H+的数目为0.001NA |
查看答案和解析>>
科目: 来源: 题型:选择题
 一定温度下,将一定量的A、B气体充入密闭容器,发生反应:A(g)+B(g)?xC(g)+3D(?),反应平衡后,改变影响平衡的一个条件,物质A的浓度变化如图所示.下列有关说法正确的是( )
一定温度下,将一定量的A、B气体充入密闭容器,发生反应:A(g)+B(g)?xC(g)+3D(?),反应平衡后,改变影响平衡的一个条件,物质A的浓度变化如图所示.下列有关说法正确的是( )| A. | x=2,C为气态,D可能为气态也可能为非气态 | |
| B. | 改变的条件可能是使用了催化剂 | |
| C. | 其他条件不变,若向容器中再加入少量C,平衡逆向移动但平衡常数不变 | |
| D. | 该反应的化学平衡常数K=$\frac{{c}^{2}(C)}{[c(A)•c(B)]}$,且温度升高,K值增大 |
查看答案和解析>>
科目: 来源: 题型:推断题
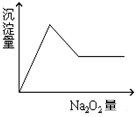 某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.
某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 呈酸性的雨水通常称为酸雨 | |
| B. | 翡翠、玛瑙、水晶等饰物都是硅酸盐制品 | |
| C. | 合金材料一定全部由金属元素组成 | |
| D. | 硅是制作太阳能电池的主要原料 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2SO4(浓)+C | B. | Fe3O4+Al | C. | Cl2+Mg | D. | NO2+H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  将NO2球浸泡在冷水中和热水中 | |||||||||||||
| B. | 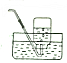 排饱和食盐水收集氯气 | |||||||||||||
| C. | 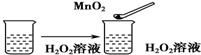 | |||||||||||||
| D. |
| |||||||||||||
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.2NA | |
| B. | 在反应KClO3+6HCl=KCl+3Cl2+3H2O中,每生成3molCl2转移的电子数为6NA | |
| C. | 含4molSi-O键的二氧化硅晶体中,氧原子数为2NA | |
| D. | 某密闭容器中盛有0.2molSO2和0.1molO2,在一定条件下充分反应,生成SO2的分子数为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com