
科目: 来源: 题型:选择题
 如图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4•10H2O)在温度为
如图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4•10H2O)在温度为| A. | 32.8g | B. | 40g | C. | 40.8g | D. | 41g |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用酚酞溶液可区别苯酚钠溶液与福尔马林 | |
| B. | 用溴水可区别丙烯与丙烯酸 | |
| C. | 用新制的Cu(OH)2悬浊液可区别醋酸与乙醇 | |
| D. | 无法用溴水除去苯中溶有的少量苯酚 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 稀有气体化学性质很稳定 | B. | 硝酸易挥发,而硫酸难挥发 | ||
| C. | 氮气的化学性质比氧气稳定 | D. | 常温常压下,溴呈液态,碘呈固态 |
查看答案和解析>>
科目: 来源: 题型:解答题
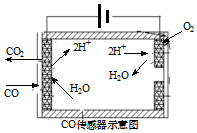 研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,二氧化锰与浓盐酸不反应,而高锰酸钾与浓盐酸反应产生氯气 | |
| B. | 接触面相近的锌粒与1mo1•L-1的盐酸反应比1mo1•L-1的硫酸反应快 | |
| C. | 同质量的煤块在空气中燃烧比煤粉燃烧要慢 | |
| D. | 甲烷与氯气的混合气体在暗室中黄绿色变浅速率比在太阳照射下慢 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 227.2kJ•mol-1 | B. | -227.2kJ•mol-1 | C. | 798.8kJ•mol-1 | D. | -798.8kJ•mol-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
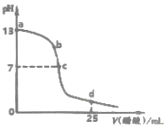 如图为常温下0.2000mol•L-1 CH3COOH溶液逐滴加入到25mL0.1000mol•L-1 NaOH溶液中pH的变化曲线,下列说法不正确的是( )
如图为常温下0.2000mol•L-1 CH3COOH溶液逐滴加入到25mL0.1000mol•L-1 NaOH溶液中pH的变化曲线,下列说法不正确的是( )| A. | a~c区间内(不包含a、c两点)可能存在:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| B. | c点时溶液中:c(Na+)=c(CH3COO-) | |
| C. | d点时溶液中:c(Na+)+c(H+)+c(CH3COO-)-c(OH-)=0.2000mol•L-1 | |
| D. | 反应过程中溶液中阴、阳离子总数:b点小于c点 |
查看答案和解析>>
科目: 来源: 题型:实验题
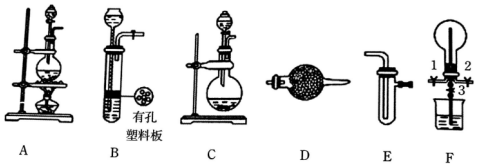
查看答案和解析>>
科目: 来源: 题型:选择题
| 编号 | 实验 | 操作 |
| A | 钠与水的反应 | 用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B | 配制一定浓度的氯化钾溶液1000mL | 准确称取氯化钾固体,放入到1000mL的容量瓶中,加水溶解,振荡摇匀,定容 |
| C | 制取Fe(OH)3胶体 | 往盛有沸水的烧杯中滴加饱和FeCl3溶液,继续煮沸并用玻璃棒不断搅拌 |
| D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体分液漏斗上端管口倒出 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com