
科目: 来源: 题型:选择题
| A. | 实验室配制FeCl3溶液时,需将FeCl3 (s)溶解在较浓盐酸中,然后加水稀释 | |
| B. | 反应2CO+2NO=N2+2CO2在常温下能自发进行,则反应△H>0,△S<0 | |
| C. | 0.1mol•L-1NH4Cl溶液加水稀释,$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$的值增大 | |
| D. | 反应CH3COOCH3+H2O?CH3COOH+CH3OH△H>0,达到平衡时,加入少量固体NaOH,则乙酸甲酯水解转化率增大 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | FeO溶于稀硝酸:FeO+2H+═Fe2++H2O | |
| B. | Al2(SO4)3溶液中加入过量Ba(OH)2溶液:Al3++4OH-═AlO2-+2H2O | |
| C. | 漂白粉溶液中通入少量CO2:2ClO-+H2O+CO2═2HClO+CO32- | |
| D. | 等物质的量的NO和NO2同时被NaOH溶液吸收:NO+NO2+2OH-═2NO2-+H2O |
查看答案和解析>>
科目: 来源: 题型:解答题
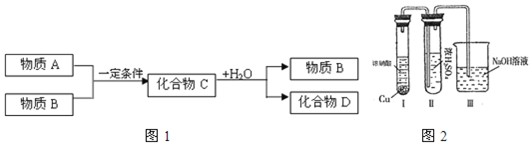
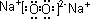 ;化合物D中所含化学键的类型是共价键、离子键.
;化合物D中所含化学键的类型是共价键、离子键.查看答案和解析>>
科目: 来源: 题型:实验题
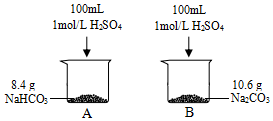 某小组同学在实验室研究Na2CO3与NaHCO3的性质.
某小组同学在实验室研究Na2CO3与NaHCO3的性质.| 实验步骤 | 实验现象 |
| ⅰ.取1mL 0.1mol/L NaHCO3溶液,向其中加入 1mL 0.01mol/L CaCl2溶液 | 无明显现象 |
| ⅱ.向上述溶液中滴加NaOH溶液 | 产生白色沉淀 |
查看答案和解析>>
科目: 来源: 题型:解答题
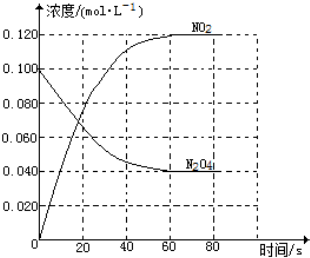 在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度的升高,混合气体的颜色变深.
在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度的升高,混合气体的颜色变深.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | FeCl3要在沸水中才能发生水解 | |
| B. | 放热反应不需要加热就能进行 | |
| C. | 将pH=2的硫酸溶液加热至100℃时pH基本不变 | |
| D. | 加热不利于合成氨,故工业上采用低温合成氨 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 碱 | 酸 | 盐 | 酸性氧化物 | |
| A | 纯碱 | 盐酸 | 胆矾 | 二氧化硫 |
| B | 烧碱 | 硫酸 | 食盐 | 一氧化碳 |
| C | 苛性钠 | 醋酸 | 石灰石 | 水 |
| D | 苛性钠 | 碳酸 | 碳酸镁 | 三氧化碳 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 某澄清透明溶液中:K+、Cu2+、NO3-、Cl- | |
| B. | 含0.1mol•L-1 Fe3+的溶液中:Na+、Mg2+、SO42-、Cl-、SCN- | |
| C. | 含0.1mol•L-1 CO32-的溶液中:OH-、Cl-、NH4+、Na+、H+ | |
| D. | 加入铝粉产生H2的溶液中:Al3+、Na+、SO42-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com