
科目: 来源: 题型:选择题
| A. | 1molNa2O2与足量H2O充分反应转移的电子数为2NA | |
| B. | 200mL,1mol/LFe2(SO4)3溶液中,Fe3+和SO42-离子总数为6.02×1023 | |
| C. | 已知2A(g)+B(g)═2C(g)△H=-akJ/mol,若将2NA个A与NA个B混合充分反应放出akJ的热量 | |
| D. | 28gSi3N4晶体中含有的硅氮键的数目为2.4NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| 操作 | 现象 | |
| A | 加入NaOH溶液 | 有红褐色沉淀 |
| B | 加入酸化的Ba(NO3)2溶液 | 有白色沉淀 |
| C | 加入酸性KMnO4溶液 | 紫色褪去 |
| D | 加入KSCN溶液 | 无明显现象 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  阿伏加德罗 | B. |  门捷列夫 | C. |  盖斯 | D. |  勒夏特列 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | AlCl3溶液中加入过量稀氨水:A13++4NH3•H2O═A1O2-+4NH4++2H2O | |
| B. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-═Fe(OH)2↓ | |
| C. | 澄清石灰水中滴加少量NaHCO3:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| D. | 溶液中加入过量的NaOH溶液:Mg2++2HCO3-+4OH-═Mg(OH)2↓+2CO32-+2H2O |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 漂白粉露置在空气中:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 用少量氨水吸收二氧化硫:SO2+NH3•H2O=HSO3-+NH4+ | |
| C. | 少量CO2通入苯酚钠溶液:2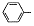 +CO2+H2O→2 +CO2+H2O→2 OH+CO32- OH+CO32- | |
| D. | 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+8H+═Fe2++2Fe3++4H2O |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 硫酸铜溶液可将方铅矿(PbS)为铜蓝(CuS) Cu2++SO42-+PbS═CuS+PbSO4 | |
| B. | 向次氯酸钙溶液中通入少量二氧化硫气体 Ca2++2 ClO-+SO2+H2O═CaSO4↓+2HClO | |
| C. | 向氢氧化钡溶液加入过量的硫酸溶液的 Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 向氯化铁溶液加入过量的硫化钠溶液 2Fe3++3S2-═2FeS↓+S↓ |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com