
科目: 来源: 题型:选择题
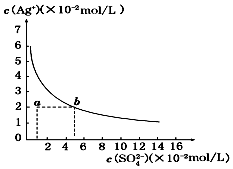
| A. | 含有大量SO42-的溶液中肯定不存在Ag+ | |
| B. | 0.02 mol/L的AgNO3溶液与0.2 mol/L的Na2SO4溶液等体积混合不会生成沉淀 | |
| C. | Ag2SO4的溶度积常数(Ksp)为1×10-3 | |
| D. | a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CH2=CH2+HBr $\stackrel{催化剂}{→}$CH3CH2Br | |
| B. | CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOC2H5 | |
| C. | 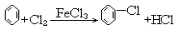 | |
| D. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Cl2$\stackrel{NaBr(aq)}{→}$Br2$\stackrel{SO_{2}(aq)}{→}$HBr | |
| B. | Fe3O4$→_{高温}^{CO}$Fe$\stackrel{HCl(aq)}{→}$FeCl3 | |
| C. | NaCl$\stackrel{NH_{4}HCO_{3}(aq)}{→}$Na2CO3$\stackrel{Ca(OH)_{2}}{→}$NaOH | |
| D. | Cu2(OH)2CO3$\stackrel{HCl(aq)}{→}$CuCl2$\stackrel{NaNO_{3}(aq)}{→}$Cu(NO3)2 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
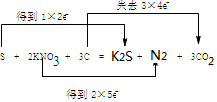 (同时用双线桥表示电子的得失)
(同时用双线桥表示电子的得失)查看答案和解析>>
科目: 来源: 题型:解答题
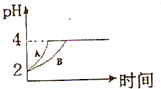 现有室温下浓度均为1×10-3mol/L的几种溶液:①盐酸、②醋酸、③氨水、④NaOH溶液,回答下列问题:
现有室温下浓度均为1×10-3mol/L的几种溶液:①盐酸、②醋酸、③氨水、④NaOH溶液,回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 含H+的物质的量,盐酸大于醋酸 | |
| B. | 分别于锌反应,产生H2的物质的量不一定相等 | |
| C. | 分别于镁反应,反应速率盐酸大于醋酸 | |
| D. | H+的物质的量浓度,盐酸大于醋酸 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 测恰好中和等体积、等物质的量浓度的甲酸和硫酸消耗NaOH的量 | |
| B. | 测甲酸和硫酸的水溶性 | |
| C. | 测相同体积不同物质的量浓度的甲酸钠和硫酸钠溶液的pH值 | |
| D. | 测相同物质的量浓度的甲酸和硫酸溶液的导电性 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | 都错误 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氢气、甲烷、乙醇在燃料电池中作负极材料 | |
| B. | 氢氧燃料电池常用于航天飞行器,原因之一是该电池的产物可回收利用 | |
| C. | 碱性介质下的乙醇燃料电池负极反应为:C2H5OH-12e-═2CO2↑+3H2O | |
| D. | 碱性介质下甲烷燃料电池的正极反应为:O2+2H2O+4e-═4OH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com