
科目: 来源: 题型:选择题
| A. | 硫酸亚铁 | B. | 还原铁粉 | C. | 亚硫酸钠 | D. | 生石灰 |
查看答案和解析>>
科目: 来源: 题型:选择题
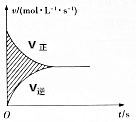 在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如图所示,则图中阴影部分的面积表示( )
在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如图所示,则图中阴影部分的面积表示( )| A. | X的浓度的变化量 | B. | Y的浓度的减小量 | ||
| C. | Z的物质的量的变化量 | D. | Y的物质的量的减小量 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2和CO | B. | CO2、H2和CO | C. | H2O | D. | H2和CO2 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒. | |
| B. | 稀释后没冷却到室温就将溶液转移至容量瓶. | |
| C. | 用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切. | |
| D. | 用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切 | |
| E. | 移液时容量瓶中有少量蒸馏水 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 浓硫酸具有吸水性,可作食品干燥剂 | |
| B. | 夏天雷雨过后感觉到空气清新是因为产生了少量NO2 | |
| C. | 缤纷绚丽的烟花中添加了含钾、钠、钙、铜等金属元素的化合物 | |
| D. | 明矾可以使海水淡化,从而解决“淡水供应危机” |
查看答案和解析>>
科目: 来源: 题型:实验题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 相同物质的量的气体摩尔体积一定相同 | |
| B. | 通常状况下的气体摩尔体积约为22.4L | |
| C. | 标准状况下的气体摩尔体积约为22.4L | |
| D. | 单位物质的量的气体所占的体积就是气体摩尔体积 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 28g N2含有的原子数为NA | |
| B. | 4gCa变成Ca2+失去的电子数为0.1NA | |
| C. | 1molO2的质量等于1mol O的质量 | |
| D. | 24gO2和24gO3所含有的原子数目相等 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com