
科目: 来源: 题型:多选题
 是一种有机烯醚,可由链烃A通过下列路线制得,下列说法正确的是( )
是一种有机烯醚,可由链烃A通过下列路线制得,下列说法正确的是( )
| A. | B中含有的官能团有溴原子、碳碳双键 | |
| B. | A的结构简式是CH2=CHCH2CH3 | |
| C. | A能使酸性高锰酸钾溶液褪色 | |
| D. | ①②③的反应类型分别为加成反应、取代反应、消去反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作及现象 |
| A | 检验1-溴丙烷中含有溴 | 将1-溴丙烷与足量氢氧化钠溶液混合加热,冷却后加硝酸银溶液,得沉淀 |
| B | 验证样品中一定含有苯酚 | 向样品溶液中滴加氯化铁溶液后显紫色 |
| C | 验证蔗糖没有水解 | 在蔗糖溶液中加入稀硫酸,水浴加热一段时间后,加入少量新制Cu(OH)2悬浊液,加热后未出现砖红色沉淀 |
| D | 证明蛋白质的变性是不可逆的 | 向蛋白质溶液中滴加CuSO4溶液,有固体析出,过滤,向固体中加足量水,固体不溶解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:多选题
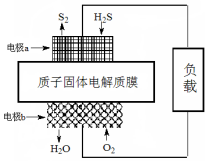 已知:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.下图为H2S燃料电池的示意图.下列说法正确的是( )
已知:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.下图为H2S燃料电池的示意图.下列说法正确的是( )| A. | 电极a为电池的负极 | |
| B. | 电极b上发生的电极反应为:O2+2H2O+4e-═4OH- | |
| C. | 电路中每通过4 mol电子,电池内部释放632 kJ热能 | |
| D. | 每34 g H2S参与反应,有2 mol H+经质子膜进入正极区 |
查看答案和解析>>
科目: 来源: 题型:多选题
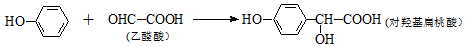
| A. | 上述反应的原子利用率可达100% | |
| B. | 上述反应类型为取代反应 | |
| C. | 对羟基扁桃酸可发生加成反应、取代反应和缩聚反应 | |
| D. | 1 mol对羟基扁桃酸与足量NaOH溶液反应,最多可消耗3 mol NaOH |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡静置后,分液 | |
| B. | 苯(苯酚):加入浓溴水,过滤 | |
| C. | 乙醇(水):加入金属钠,蒸馏 | |
| D. | 乙烷(乙烯):通入酸性高锰酸钾溶液,洗气 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙醇与浓氢溴酸反应:CH3CH2OH+HBr $\stackrel{△}{→}$CH3CH2Br+H2O | |
| B. | 溴乙烷与氢氧化钠溶液共热:CH3CH2Br+NaOH$\stackrel{△}{→}$CH3CH2OH+NaBr | |
| C. | 苯酚钠溶液中通入少量二氧化碳: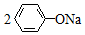 +CO2→ +CO2→ +Na2CO3 +Na2CO3 | |
| D. | 蔗糖在稀硫酸作用下水解:C12H22O11(蔗糖)+H2O$→_{△}^{稀硝酸}$C6H12O6(葡萄糖)+C6H12O6(果糖) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用聚氯乙烯树脂生产食品包装袋 | |
| B. | 用工业酒精勾兑白酒 | |
| C. | 合理利用可燃冰有利于弥补能源短缺 | |
| D. | 用含甲酚的药皂除菌消毒,是利用酚类物质的强氧化性 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 元素C位于周期表中第三周期ⅢA族 | |
| B. | 电解熔融化合物CE3可制取单质C | |
| C. | D的最高价含氧酸的浓溶液与单质A共热时能生成三种氧化物 | |
| D. | 化合物B2D2中既含离子键又含非极性共价键 |
查看答案和解析>>
科目: 来源: 题型:计算题
| 物质 | X | Y | Z |
| 初始浓度(mol/L) | 0.1 | 0.2 | 0 |
| 平衡浓度(mol/L) | 0.05 | 0.05 | 0.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com