
科目: 来源: 题型:选择题
| A. | 在H2O2+Cl2═2HCl+O2反应中,每生成32 g氧气,转移4NA个电子 | |
| B. | 标准状况下,22.4 L CCl4中含有CCl4的分子数为NA | |
| C. | 50 mL 12 mol/L盐酸与足量MnO2共热,转移的电子数为0.5NA | |
| D. | 一定条件下,2.3 g Na完全与O2反应生成3.6 g产物时失去的电子数为0.1NA |
查看答案和解析>>
科目: 来源: 题型:选择题
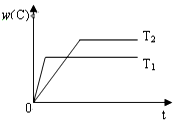 对于反应A(g)+2B(g)?2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示.则下列结论正确的是( )
对于反应A(g)+2B(g)?2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示.则下列结论正确的是( )| A. | T1>T2,正反应放热 | B. | T1<T2,正反应放热 | ||
| C. | T1>T2,正反应吸热 | D. | T1<T2,正反应吸热 |
查看答案和解析>>
科目: 来源: 题型:选择题
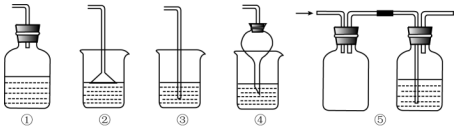
| A. | ②④⑤ | B. | ①②④ | C. | ①②③ | D. | ①②④⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 配制过程只需要三种仪器即可完成 | |
| B. | 容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制 | |
| C. | 所配得的NaClO消毒液物质的量浓度为3.99mol/L | |
| D. | 需要称量的NaClO固体的质量为140g |
查看答案和解析>>
科目: 来源: 题型:实验题
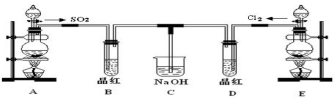
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 升高温度,活化分子百分数增大,正、逆反应速率都加快 | |
| B. | 使用催化剂,活化分子百分数增大,正、逆反应速率都加快 | |
| C. | 使用催化剂可以降低反应的活化能 | |
| D. | 升高温度,上述反应的平衡常数会增大 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | SO42-的空间构型是正四面体形 | |
| B. | CS2分子中各原子均达8电子稳定结构 | |
| C. | 甲醛分子中碳原子的杂化类型为sp2 | |
| D. | CO2与SO2为等电子体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.1 mol NaHSO4晶体中含阴阳离子总数是0.3NA | |
| B. | 将0.1mol FeCl3加到沸水中制得的胶体中,含胶粒0.1NA | |
| C. | 1 mol Na2O2与足量H2O完全反应,转移电子数目为2NA | |
| D. | 在常温常压下,13.8g NO2与足量水充分反应,剩余气体的分子数为0.1NA |
查看答案和解析>>
科目: 来源: 题型:实验题
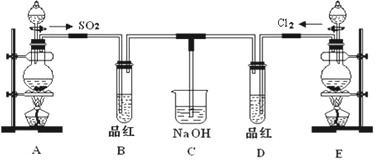
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com