
科目: 来源: 题型:解答题
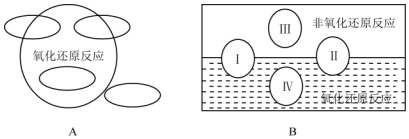 氧化还原是常见的反应类型,根据信息回答以下问题:
氧化还原是常见的反应类型,根据信息回答以下问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na+与N3-的电子层结构都与氩原子相同 | |
| B. | Na3N中的Na+的半径大于N3-的半径 | |
| C. | Na3N与盐酸反应可生成两种盐 | |
| D. | Na3N与水的反应属于氧化还原反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 测量氯化钠的熔点 | B. | 测量固体氯化钠的导电性 | ||
| C. | 测量熔融氯化钠的导电性 | D. | 测量氯化钠水溶液的导电性 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1mol二氧化碳在标准状况时所占的体积约是22.4L | |
| B. | 氧气在标准状况下頕有体积约为22.4L | |
| C. | 1mol任何物质在0℃,1.01×105Pa时体积都约是22.4L | |
| D. | 1mol任何气体的体积都约是22.4L |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 提取食盐后的母液$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{稀HCl}{→}$MgCl2溶液$\stackrel{电解}{→}$Mg | |
| B. | Cu$\stackrel{H_{2}O_{2},稀H_{2}SO_{4}}{→}$CuSO4溶液$\stackrel{蒸发,结晶}{→}$CuSO4•5H2O | |
| C. | 饱和食盐水$\stackrel{NH_{3}}{→}$$\stackrel{CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| D. | N2$→_{催化剂}^{H_{2}}$NH3$→_{催化剂}^{O_{2}}$NO→NO2$\stackrel{H_{2}O}{→}$HNO3 |
查看答案和解析>>
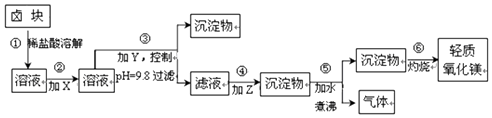
科目: 来源: 题型:实验题
| 表1:生成氢氧化物沉淀的pH | 表2:原料价格表 | |||
| 物质 | 开始沉淀 | 沉淀完全 | 物质 | 价格(元/吨) |
| Fe(OH)3 | 2.7 | 3.7 | a.漂液(含25.2%NaClO) | 450 |
| Fe(OH)2 | 7.6 | 9.6﹡ | b.双氧水(含30%H2O2) | 2400 |
| 资*源%库Mn(OH)2 | 8.3 | 9.8 | c.烧碱(含98%NaOH) | 2100 |
| Mg(OH)2 | 9.6 | 11.1 | d.纯碱(含99.5%Na2CO3) | 600 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com