
科目: 来源: 题型:选择题
| A. | 溶解度(s ) | B. | 物质的量浓度(c ) | C. | 质量分数(w%) | D. | 摩尔质量(M ) |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 如图 1 所示,若铜中含有杂质银,可形成原电池,且铜作负极 | |
| B. | 如图 2 所示,当有 0.1 mol 电子转移时,有 0.1 mol Cu2O 生成 | |
| C. | 基于绿色化学理念设计的制取 Cu2O 的电解池如图 2 所示,铜电极发生还原反应 | |
| D. | 若图 3 所示的装置中发生 Cu+2Fe3+═Cu2++2Fe2+的反应,则 X 极是负极,Y 极的材料可 以是铜 |
查看答案和解析>>
科目: 来源: 题型:选择题
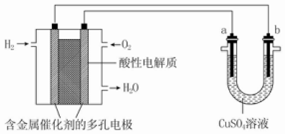
| A. | 燃料电池工作时,正极反应为 O2+2H2O+4e═4OH | |
| B. | a 极是铁,b 极是铜时,b 极逐渐溶解,a 极上有铜析出 | |
| C. | a 极是粗铜,b 极是纯铜时,a 极逐渐溶解,b 极上有铜析出 | |
| D. | a、b 两极均是石墨时,在相同条件下 a 极产生的气体与电池中消耗的 H2 体积相等 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN浓液 | 有气体生成,溶液未呈红色 | 稀硝酸不能将Fe氧化为Fe3+ |
| B | NaAlO2溶液中滴入NaHCO3溶液 | 产生白色沉淀 | AlO2-与HCO3-发生双水解反应 |
| C | 向某溶液里滴加NaOH溶液并将湿润的红色石蕊试纸置于试管口 | 试纸颜色没变 | 原溶液中无NH4- |
| D | 将0.1mol/LMgSO4溶液滴入NaOH溶液里至不再有沉淀产生,再滴加0.1mol/LCuSO4溶液 | 先有白色沉淀生成,后变为蓝色沉淀 | Cu(OH)2的Ksp小于Mg(OH)2的Ksp |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | |
| B. | 铝和氢氧化钠水溶液反应:Al+2OH-+2H2O═AlO2-+3H2↑ | |
| C. | 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH- $\frac{\underline{\;△\;}}{\;}$NH3↑+H2O | |
| D. | AlCl3溶液中滴加足量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ca(HCO3)2溶液与足量NaOH溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+H2O | |
| B. | 等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| C. | 向100mL 1mol/L FeBr2溶液中通入0.5mol Cl2:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 氢氧化铁与足量的氢溴酸溶液反应:Fe(OH)3+3H+═Fe3++3H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 12g的金刚石晶体中含有碳碳键的数目为4NA | |
| B. | 46g四氧化二氮含有的原子总数一定为3NA | |
| C. | 500mLl.0mol/L的乙酸溶液中含有的H+数为0.5NA | |
| D. | 1 molFeCl3制成胶体,所得胶体的粒子数为NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 二氧化硅与氧化钙(高温) | B. | 二氧化硅与氢氧化钠(常温) | ||
| C. | 二氧化硅与碳(高温) | D. | 二氧化硅与浓HNO3(常温) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com