
科目: 来源: 题型:实验题
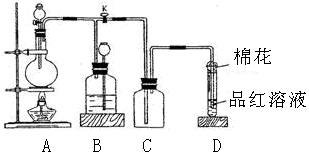
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 胶体带电荷,溶液不带电荷 | |
| B. | 胶体区别于其它分散系的本质特征是分散质的直径大小 | |
| C. | 将一柬光线通过胶体时可出现一条光亮的通路,通过溶液则没有此现象 | |
| D. | 土壤胶粒的表面巨大且带负电,能吸附NH${\;}_{4}^{+}$等营养离子,使土壤具有保肥能力 |
查看答案和解析>>
科目: 来源: 题型:实验题
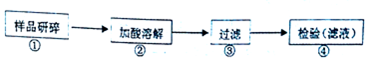
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 元素周期表中有7个主族,7个副族,共14个纵行 | |
| B. | 氮元素位于第二周期第三主族 | |
| C. | 金属性最强的元素是Li | |
| D. | 非金属性最强的元素是F |
查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:实验题
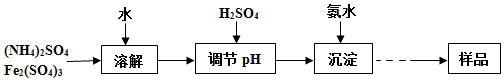
查看答案和解析>>
科目: 来源: 题型:解答题
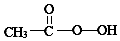 )常用作纺织品漂白剂.
)常用作纺织品漂白剂.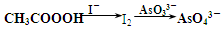
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com