
科目: 来源: 题型:选择题
| A. | 碳酸钙溶于稀盐酸中Ca CO3+2 H+═H2O+CO2↑+Ca2+ | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2 H+═Ca2++2 H2O | |
| C. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO2↑+H2O | |
| D. | 氢氧化镁与盐酸的反应OH-+H+═H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在KClO3+6HCl=3Cl2↑+KCl+3H2O中,被氧化的氯原子和被还原的氯原子的个数比为6:1 | |
| B. | 在反应:2KNO3+3C+S=K2S+N2↑+3CO2↑,则被还原的元素为氮和硫 | |
| C. | 失电子能力难的原子获得电子的能力一定强 | |
| D. | 在化学反应中某元素由化合态变为游离态,该元素一定被还原了 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 碱性氧化物一定是金属氧化物,金属氧化物一定是碱性氧化物 | |
| B. | 由一种元素组成的物质一定是单质,两种元素组成的物质一定是化合物 | |
| C. | 非金属氧化物不一定是酸性氧化物,酸性氧化物不一定都是非金属氧化物 | |
| D. | 硫酸、纯碱、石膏是按酸、碱、盐排列的 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 能用分液漏斗分离碘和四氯化碳的混合物 | |
| B. | 蒸发操作时,应使混合物中的水份完全蒸干后,才能停止加热 | |
| C. | 分液操作时,下层液体从分液漏斗下口放出,上层液体从下口放出到另一个烧杯中 | |
| D. | 实验室取用液体药品做实验时,如没有说明用量,一般取1---2mL |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①② | B. | ①②③ | C. | ①②③④ | D. | 全部 |
查看答案和解析>>
科目: 来源: 题型:实验题
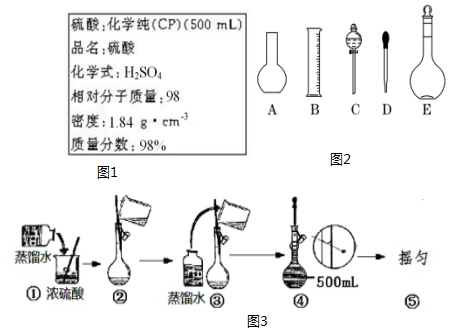
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 40.75 | B. | 29.38 | C. | 14.69 | D. | 无法计算 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com