
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A | B | C | D |
| 向一定量石灰石中滴加稀盐酸 | 向一定量硫酸铜溶液中不断加入铁粉 | 向足量盐酸中加等量的金属Zn、Fe | 向一定量过氧化氢溶液中加入少量二氧化锰 |
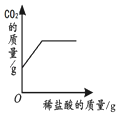 | 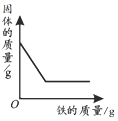 | 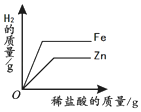 | 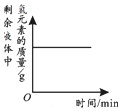 |
| A. | A | B. | B | C. | C | D. | DA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①和④ | B. | ②和③ | C. | ②③④ | D. | 只有④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向上述溶液中滴加几滴NaOH溶液,溶液颜色会加深,因为OH-与Fe3+生成了红褐色沉淀 | |
| B. | 向上述溶液中滴加几滴NaOH溶液,溶液颜色会变浅,因为OH-与Fe3+生成了红褐色沉淀,使Fe3+的浓度减小,平衡逆向移动,导致Fe(SCN)3的浓度减小 | |
| C. | 向上述溶液中滴加几滴1 mol/L KSCN溶液,溶液颜色会加深,因为SCN-的浓度增大,正反应速率加快,平衡正向移动,导致导致Fe(SCN)3的浓度增大 | |
| D. | 向上述溶液中分别滴加NaOH溶液和KSCN溶液过程中,Na+、K+的浓度大小对平衡体系没有影响 |
查看答案和解析>>
科目: 来源: 题型:推断题
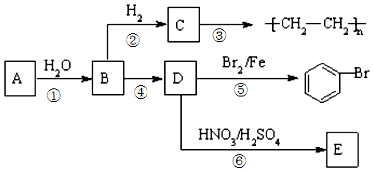
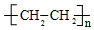 ;⑥
;⑥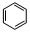 +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$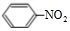 +H2O.
+H2O. ;
; .
.查看答案和解析>>
科目: 来源: 题型:实验题
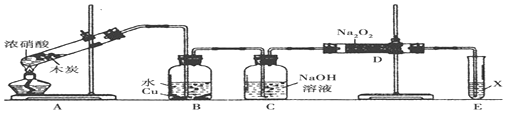
查看答案和解析>>
科目: 来源: 题型:推断题
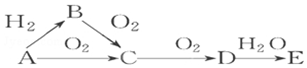 已知A是气体单质,E的水溶液显强酸性.A、B、C、D、E是含有一种相同元素的五种物质,在一定条件下可发生如图所示的转化.
已知A是气体单质,E的水溶液显强酸性.A、B、C、D、E是含有一种相同元素的五种物质,在一定条件下可发生如图所示的转化.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在常温常压下,11.2 LN2含有的分子数为0.5 NA | |
| B. | 71gCl2所含原子数为NA | |
| C. | 在常温常压下,1molNe含有的原子数为NA | |
| D. | 在同温、同压下,相同体积的任何气体单质所含的原子数相同 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 2 L溶液中Ba2+和Cl-的总数为0.8NA | |
| B. | 500 mL溶液中Cl-的浓度为0.2 mol•L-1 | |
| C. | 500 mL溶液中Ba2+的浓度为0.2 mol•L-1 | |
| D. | 500 mL溶液中Cl-的总数为0.2NA |
查看答案和解析>>
科目: 来源: 题型:实验题
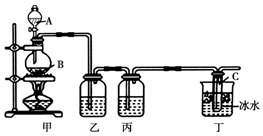 某化学活动小组欲用如图所示装置进行实验制取漂白液(次氯酸钠和氯化钠的混合溶液),并提高次氯酸钠含量.图中瓶乙盛饱和食盐水,瓶丙盛浓硫酸,分液漏斗A中盛浓盐酸.(据资料显示:Cl2和NaOH在不同温度下,产物不同.在较高温度下易生成NaClO3)试回答:
某化学活动小组欲用如图所示装置进行实验制取漂白液(次氯酸钠和氯化钠的混合溶液),并提高次氯酸钠含量.图中瓶乙盛饱和食盐水,瓶丙盛浓硫酸,分液漏斗A中盛浓盐酸.(据资料显示:Cl2和NaOH在不同温度下,产物不同.在较高温度下易生成NaClO3)试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com