
科目: 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:选择题
某稀硫酸和稀硝酸的混合溶液中c(SO42-)+ c(NO3-)=2.5 mol•L-1,取200mL该混合酸,则能溶解铜的最大质量为
A.12.8 g B. 19.2 g C. 32.0 g D. 38.4 g
查看答案和解析>>
科目: 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:选择题
已知:还原性HSO3->I-,氧化性IO3->I2。在含3 mol NaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图(不考虑I2+I-  I3-)下列说法不正确的是
I3-)下列说法不正确的是
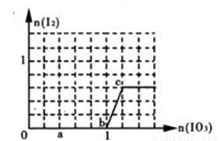
A.a点时消耗NaHSO3的物质的量为1.2mol,得到的氧化产物为SO42-
B.b~c段的反应可用如下离子方程式表示:IO3-+5I-+6H+=3I2+3H2O
C.滴加过程中水的电离平衡一直逆向移动。
D.从c点后所得混合液中分离出碘的操作为:加四氯化碳萃取分液,然后蒸馏
查看答案和解析>>
科目: 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:实验题
I.高锰酸钾溶液常用于物质的定性检验与定量分析。
(1)实验室里欲用KMnO4固体来配制480mL 0.1000 mol·L-1的酸性KMnO4溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、 。
②下列操作对实验结果的影响偏大的是 (填序号)。
a.加水定容时俯视刻度线
b.容量瓶底部有少量蒸馏水
c.颠倒摇匀后发现凹液面低于刻度线又加水补上
d.天平的砝码生锈
(2)某化学兴趣小组,用新配制的酸性KMnO4溶液来测定某试剂厂生产的FeSO4溶液中Fe2+的物质的量浓度。
①酸性高锰酸钾溶液与FeSO4溶液反应的离子方程式为
②该小组在测定过程中发现,测得的Fe2+的物质的量浓度比标签上的标注值要低,在滴定操作准确的前提下,可能导致该测定结果的原因如下:
猜想一:FeSO4溶液变质;证明方法是
猜想二:
Ⅱ.某强酸性反应体系中,反应物和生成物共六种物质:PbO2、PbSO4(难溶盐)、Pb(MnO4)2(强电解质)、H2O、X(水溶液呈无色)、H2SO4,已知X是一种盐,且0.1 mol X在该反应中失去3.01×1023个电子。
(1)写出该反应的化学方程式:________________________;
(2)该反应体系中,若用浓盐酸代替硫酸,用离子方程式表示后果: 。
查看答案和解析>>
科目: 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:实验题
铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的工艺如下(部分操作和条件略):
Ⅰ.将铬铁矿和碳酸钠混合在空气中充分焙烧。
Ⅱ.焙烧后的固体加水浸取,分离得到溶液A和固体A。
Ⅲ.向溶液A中加入醋酸调pH约7~8,分离得到溶液B和固体B。
Ⅳ.再向溶液B中继续加醋酸酸化,使溶液pH小于5。
Ⅴ.向上述溶液中加入氯化钾,得到重铬酸钾晶体。
(1)Ⅰ中焙烧发生的反应如下,配平并填写空缺:
① FeO•Cr2O3 + Na2CO3 + □ = Na2CrO4 + Fe2O3 + CO2↑
② Na2CO3+Al2O3=2NaAlO2+CO2↑
(2)固体A中主要含有 (填写化学式)。
(3)Ⅴ中发生反应的化学方程式是:Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl,已知下表数据
物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
溶解度 (g/100g水) | 0℃ | 28 | 35.7 | 4.7 | 163 |
40℃ | 40.1 | 36.4 | 26.3 | 215 | |
80℃ | 51.3 | 38 | 73 | 376 | |
获得K2Cr2O7晶体的操作由多步组成,依次是:加入KCl固体、 、过滤、洗涤、干燥得到晶体。洗涤沉淀的操作为 。
(4)Ⅲ中固体B中主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析固体B中氢氧化铝含量的方法是:称取n g样品,加入过量 (填写试剂名称)、溶解、过滤、再通入过量的CO2、灼烧、冷却、称量,得干燥固体m g。计算样品中氢氧化铝的质量分数为 (用含m、n的代数式表示)。
查看答案和解析>>
科目: 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:实验题
某研究所对含硫酸亚铁和硫酸铜的工业废料进行相关的研究。实验过程如下:
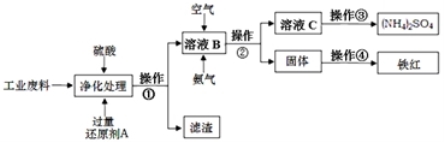
回答下列问题:
(1)滤渣的成分为 ,操作①的名称为 。
(2)上图溶液B中所发生反应的离子方程式为 。
(3)实验要求向溶液B中通入过量的空气,证明通入空气过量的方法是 。
(4)操作③第一步需要的仪器除了酒精灯、铁架台外,还需要 。
(5)某同学利用下面装置制备氢气并利用氢气还原某金属氧化物,根据要求回答问题。
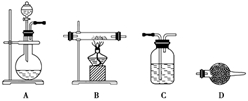
①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是A→________→________→________→D(除D装置外,其它装置不能重复使用),最后D装置中所加药品为_______________,其作用是___________________。
②点燃B处酒精灯之前必须进行的操作是 。
查看答案和解析>>
科目: 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:填空题
I. 三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
(1)反应过程中,被氧化与被还原的元素原子的物质的量之比为 。
(2)写出该反应的化学方程式_________________,若反应中生成0.2 mol HNO3,转移的电子数目为____________个。
(3)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现,你判断该气体泄漏时的现象是 。
(4)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO2、NaF、H2O外,还肯定有__________(填化学式) 。
II.(1)已知Fe(OH)3能与次氯酸盐发生如下反应(未配平):Fe(OH)3+ClO-+OH-→FeO4n-+Cl-+H2O
①已知有10.7 g Fe(OH)3参加反应,共转移了0.3NA个电子,则n = ,FeO4n- 中铁元素的化合价为 。
② 根据所学的知识,推测FeO4n- 能和下列 (填序号)物质反应。
A.KMnO4 B.SO2 C.H2S D.O2
(2)一定条件下,含硝酸的废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH,转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比是 。
查看答案和解析>>
科目: 来源:2017届四川省高三上10月月考化学试卷(解析版) 题型:选择题
化学与生活、社会密切相关,下列说法错误的是( )
A.过氧化钠可作航天员和潜水员的供氧剂
B.NaNO2可防止食物腐败,腌腊制品中的NaNO2对人体没有副作用
C.干冰和碘化银均可用于人工降雨
D.高铁车厢大部分材料采用铝合金,因为铝合金强度大、质量轻、抗腐蚀能力强
查看答案和解析>>
科目: 来源:2017届四川省高三上10月月考化学试卷(解析版) 题型:选择题
下列关于物质分类的说法正确的是( )
A.根据不同的分类标准,可将盐酸归类为纯净物、一元酸、强电解质
B.糖类、油脂、蛋白质都属于天然高分子化合物
C.根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸和多元酸
D.物质的分解、水解、裂解、电解均属于常见的化学变化
查看答案和解析>>
科目: 来源:2017届四川省高三上10月月考化学试卷(解析版) 题型:选择题
下列离子反应方程式正确的是( )
A.向Na2SiO3溶液中逐滴加入少量稀盐酸:SiO32-+ 2H+=H2SiO3(胶体)
B.将Cu片加入稀硝酸中:Cu + 4H++2NO3-=Cu2+ +2NO2↑+ 2H2O
C.向Na2S2O3溶液中加入稀硫酸:2S2O32-+2H+=SO42-+3S↓+H2O
D.向NH4Al(SO4) 2溶液中滴入Ba(OH)2恰好使SO42-反应完全:
2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O
查看答案和解析>>
科目: 来源:2017届四川省高三上10月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.40g碳化硅晶体中含有的C—Si的数目为2NA
B.1L 1 mol·L-1 AlCl3溶液中含有的Al3+数目为NA
C.0.1mol熔融的NaHSO4中含有的阳离子为0.2 NA个
D.在标况下,11.2L HCHO中含有π键的数目为0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com