
科目: 来源: 题型:选择题
| A. | 简单离子半径:W>Z>X | |
| B. | X、Y、Z都能与W组成离子化合物 | |
| C. | X、Y组成的化合物可与W单质反应 | |
| D. | Q是Z、W组成的化合物,1molQ中约含有6.02×1023个阴离子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 质子数:d>c>b>a | B. | 离子半径:W2+>X+>Y2->Z- | ||
| C. | 原子半径:Z<Y<W<X | D. | 最低负价:X<W<Z<Y |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | Z为金属 | |
| B. | WY比WR稳定 | |
| C. | X的最高价氧化物对应的水化物为弱酸 | |
| D. | XR3是离子化合物 |
查看答案和解析>>
科目: 来源: 题型:解答题
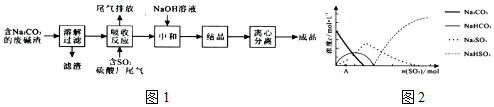
查看答案和解析>>
科目: 来源: 题型:实验题
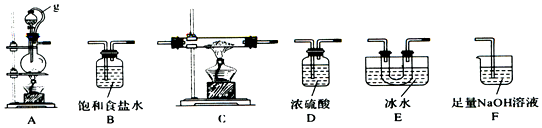
| 实验序号 | 0.1mol/L NaClO溶液/mL | 0.1mol/L NaCl溶液/mL | 0.2mol/L NaOH溶液/mL | H2O/mL | 品红溶液 | 现象 |
| ① | 4.0 | 0 | 0 | 4.0 | 3滴 | 较快褪色 |
| ② | 0 | 4.0 | 4.0 | 0 | 3滴 | 不褪色 |
| ③ | 4.0 | 0 | 4.0 | 0 | 3滴 | 缓慢褪色 |
查看答案和解析>>
科目: 来源: 题型:选择题
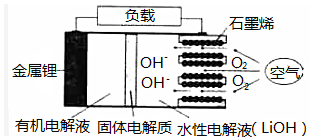 新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )
新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )| A. | 放电时,负极反应式:Li-e-+OH-═LiOH | |
| B. | 放电时,当外电路中有1mole-转移时,水性电解液离子总数增加NA | |
| C. | 应用该电池电镀铜,阴极质量增加64g,理沦上将消耗11.2LO2 | |
| D. | 若把水性电解液换成固体氧化物电解质,则易引起正极材料碳孔堵塞 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| ① | 检验淀粉是否水解生成葡萄糖 | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后新制Cu(OH)2浊液,加热,观察是否有红色沉淀生成 |
| ② | 比较H2CO3,HCN的酸性强弱 | 用pH计测定同温度同浓度的Na2CO3溶液和NaCN溶液的pH,比较pH大小 |
| ③ | 区别植物油和矿物油 | 向植物油和矿物油中分别加入烧碱溶液,加热,冷却后观察是否分层 |
| ④ | 验证CaCO3的溶解度小于CaSO4 | 将浓Na2CO3溶液滴加到CaSO4悬浊液中,充分振荡,过滤、洗涤,向所得固体中滴加盐酸,观察是否有气体生成 |
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①③ |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 若图中均为非氧化还原反应,当丁为一元强碱时,甲可能是NaAlO2 | |
| B. | 若图中均为非氧化还原反应,当丁为一元强酸时,甲可能是NaOH | |
| C. | 若图中均为氧化还原反应,当丁为非金属单质时,丙可能是NH3 | |
| D. | 若图中均为氧化还原反应,当丁为金属单质时,丙可能是FeCl3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在浓硫酸作用下,60g冰醋酸与足量无水乙醇反应生成乙酸乙酯的分子数为NA | |
| B. | 标准状况下,3.36LC2H4和C3H6的混合气体中含有碳碳双键的数目为0.15NA | |
| C. | 电解精炼铜,当外电路转移NA个电子时,阳极质量减少32g | |
| D. | 含0.01molFeCl3的浓溶液滴入沸水,制得的胶体粒子数目小于0.01NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com