
科目: 来源: 题型:选择题
| A. | 液氯较氯水的漂白作用更强 | B. | 液氯与氯水均有酸性 | ||
| C. | 液氯是纯净物,氯水是混合物 | D. | 液氯是无色的,氯水呈黄绿色 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 钠是银白色、质软、熔点相对较低、密度比水小的金属单质 | |
| B. | 大量的钠着火时可以用沙子扑灭 | |
| C. | 金属钠在空气中长期放置,最终变为碳酸钠 | |
| D. | 过氧化钠是白色固体 |
查看答案和解析>>
科目: 来源: 题型:多选题
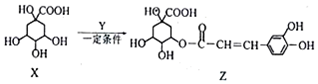
| A. | X能使酸性高锰酸钾溶液褪色 | |
| B. | Y的分子式为C9H8O3 | |
| C. | 1mol Z与足量NaOH溶液反应,最多消耗8mol NaOH | |
| D. | Z与浓溴水既能发生取代反应又能发生加成反应 |
查看答案和解析>>
科目: 来源: 题型:推断题
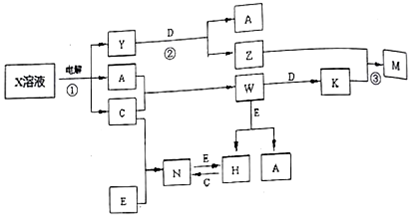
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 生成42.0LN2(标准状况) | |
| B. | 被氧化的N原子的物质的量为3.75mol | |
| C. | 有0.250mol KNO3被氧化 | |
| D. | 转移电子的物质的量为1.75mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该磁黄铁矿中FexS的x=0.425 | |
| B. | 生成的H2S气体在标准状况下的体积为2.24L | |
| C. | 100mL的盐酸中HCl物质的量浓度为8.5mol/L | |
| D. | 该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为3:1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 20℃时,饱和NaCl溶液的溶解度:S=$\frac{5850c}{ρ-58.5}$g | |
| B. | 此溶液中NaCl的质量分数为:$\frac{58.5×c}{ρ×1000}$×100% | |
| C. | 20℃时,密度小于ρ g•cm-3的NaCl溶液是不饱和溶液 | |
| D. | 温度低于20℃时,饱和NaCl溶液的浓度小于cmol•L-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na+ | B. | SO42- | C. | Ba2+ | D. | NH4+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 25℃时,0.1mol•L-1HF溶液中pH=1 | |
| B. | 向AgI饱和溶液中加入NaCl溶液,不会有AgCl沉淀析出 | |
| C. | 25℃时,使AgCl转化为AgI,则加入KI溶液的浓度不低于5×10-12mol/L | |
| D. | 向1L 0.1mol/LHF溶液中加入1L 0.1mol/LCaCl2溶液,没有沉淀产生 |
查看答案和解析>>
科目: 来源: 题型:选择题
| Ⅰ操作 | Ⅱ结论 | |
| A | 滴加BaC12溶液生成白色沉淀 | 原溶液中有SO42- |
| B | 用洁净铂丝蘸取溶液进行焰色反应:火焰呈黄色 | 原溶液中有Na+无K+ |
| C | 滴加氯水和CC14,振荡、静置.下层溶液显紫色 | 原溶液中一定有KI |
| D | 向盐溶液中滴加几滴浓NaOH溶液,微热,再将湿润红色石蕊试纸置于试管口,试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com