
科目: 来源: 题型:选择题
| A. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| B. | 合成洗涤剂和纯碱溶液都可洗去油污的原理相同 | |
| C. | 纤维素食用在人体内水解为葡萄糖为人体提供能量 | |
| D. | SO2具有还原性,可用已知浓度的KMnO4溶液测定食品中SO2残留量 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 使用含有氯化钙的融雪剂会加速桥梁的腐蚀 | |
| B. | 雾霾是一种分散系,N95活性炭口罩可用于防霾,其原理是吸附作用 | |
| C. | 大力推广使用煤的液化、气化技术,能减少二氧化碳的排放 | |
| D. | 晶体硅制得的光电池,能直接将光能转化为电能 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验操作 | 解释或结论 |
| A | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 | Fe(OH)3的溶解度小于Mg(OH)2的 |
| B | 用蒸馏水润湿的pH试纸测溶液的pH | 一定会使测定结果偏低 |
| C | 测定中和热时,使用碎泡沫起隔热保温的作用,用普通玻璃棒进行搅拌使酸和碱充分反应,准确读取实验时的最高温度并且取2~3次的实验平均值等,以达到良好的实验效果 | 用简易量热计测定反应热 |
| D | 用氢氧化钾与浓硫酸测定中和反应的反应热 | 测得的结果偏小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用分液漏斗分离除去溴苯中混入的溴 | |
| B. | 顺-2-丁烯和反-2-丁烯的加氢产物不同 | |
| C. | 石油的裂解是化学变化,而石油的分馏和煤的干馏是物理变化 | |
| D. | 结构简式为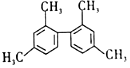 的分子中至少有11个碳原子处于同一平面上 的分子中至少有11个碳原子处于同一平面上 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | Al2O3(Fe2O3)用盐酸 | B. | Al2O3(SiO2)用氢氧化钠溶液 | ||
| C. | NaHCO3溶液(Na2CO3)通入过量CO2 | D. | NaHCO3溶液(Na2SiO3)通入过量CO2 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CO32-+2H2O?H2CO3+2OH- | |
| B. | CH3COOH+OH-═CH3COO-+H2O | |
| C. | 碳酸氢钠溶液:HCO3-+H2O?CO32-+H3O+ | |
| D. | Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3H+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加压 | B. | 增大体积 | C. | 减少A的浓度 | D. | 降温 |
查看答案和解析>>
科目: 来源: 题型:解答题
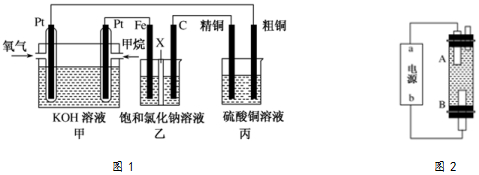
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com