
科目: 来源: 题型:解答题
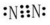 .
.查看答案和解析>>
科目: 来源: 题型:推断题
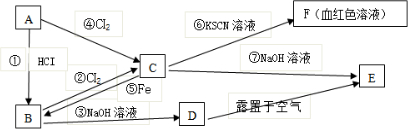
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙醇和乙酸都是常用调味品的主要成分 | |
| B. | 乙醇和乙酸的沸点和熔点都比C2H6和C2H4的沸点和熔点高 | |
| C. | 乙酸和乙醇之间能发生酯化反应 | |
| D. | 乙醇 和乙酸都能发生消去反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
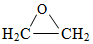 +CaCl2+2H2O
+CaCl2+2H2O +CaCl2+H2O
+CaCl2+H2O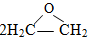
| A. | 12.7% | B. | 25.4% | C. | 50.8% | D. | 76.2% |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.2 mol过氧化氢完全分解转移的电子数目为0.4NA | |
| B. | 300 mL 2 mol/L蔗糖溶液中所含分子数为0.6 NA | |
| C. | 在常温常压下,17 g硫化氢所含质子数目为8 NA | |
| D. | 在标准状况下,2.24 L二氧化硫与氧气混合气体中所含氧原子数为0.2 NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 国际单位制中的一个物理量 | B. | 摩尔是表示物质的量 | ||
| C. | 摩尔是物质的量的单位 | D. | 摩尔是表示物质数量的单位 |
查看答案和解析>>
科目: 来源: 题型:解答题
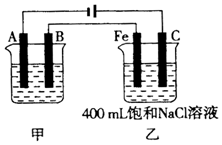 如图为相互串联的甲、乙两电解池.
如图为相互串联的甲、乙两电解池.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  可用装置鉴别碳酸钠和碳酸氢钠 | |
| B. | 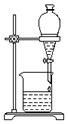 可用装置分离汽油和水的混合物 | |
| C. | 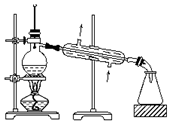 可用装置从海水中蒸馏得到淡水 | |
| D. | 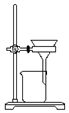 可用装置把胶体粒子从分散系中分离出来 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③⑤⑥ | B. | ②④⑤⑥ | C. | 只有⑤ | D. | 只有⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com