
科目: 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 检验Fe(NO3)2样品已被氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 |
| B | 提取碘水中碘 | 将碘水倒入分液漏斗,加入适量乙醇,振荡后静置 |
| C | 验证Mg(OH)2沉淀可以转化为 Fe(OH)3沉淀 | 向 2mL1mol•L-1NaOH 溶液中加入2~3 滴 lmol•L-1MgCl2溶液,生成白色沉淀,再加入2~3滴lmol•L-1FeCl3溶液 |
| D | 比较碳和硅的非金属性强弱 | 向饱和的Na2SiO3溶液中通人CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 放电过程中Li+向正极移动 | |
| B. | 可加入硫酸以提高电解质的导电性 | |
| C. | 充电时,Li+向阳极移动 | |
| D. | 放电时,负极反应式为:2Li0.35NiO2+Li++e-═2Li0.85NiO2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 单位时间内生成CO和Cl2的物质的量比为1:1时,反应达到平衡状态 | |
| B. | 用催化剂能提高反应物的平衡转化率 | |
| C. | 平衡时其他条件不变,升高温度能提高COCl2的转化率 | |
| D. | 当反应达平衡时,恒温恒压条件下通入Ar能提高COCl2的转化率 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加少量水 | B. | 加少量NaOH固体 | C. | 加少量浓氨水 | D. | 通入少量HCl气体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | .原子半径X>Y>Z | |
| B. | .非金属性 X>Y>Z | |
| C. | 气态氢化物的稳定性按X、Y、Z顺序由弱到强 | |
| D. | .阴离子的还原性按X、Y、Z顺序由强到弱 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 放电时,Co元素的化合价升高 | |
| B. | 放电时,正极的电极反应式为Lil-xCoO2+xe-+xLi+=LiCoO2 | |
| C. | 充电时,Li+在电解质中由阳极向阴极迁移 | |
| D. | 充电时,阴极的电极反应式为C6+xLi++xe-=LixC6 |
查看答案和解析>>
科目: 来源: 题型:多选题
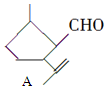 ,下列检验A中官能团的试剂和顺序正确的是( )
,下列检验A中官能团的试剂和顺序正确的是( )| A. | 先加溴水,再加KMnO4酸性溶液 | |
| B. | 先加入足量的新制Cu(OH)2悬浊液,微热,酸化后再加溴水 | |
| C. | 先加银氨溶液,微热,再加溴水 | |
| D. | 先加KMnO4酸性溶液,再加银氨溶液,微热 |
查看答案和解析>>
科目: 来源: 题型:选择题
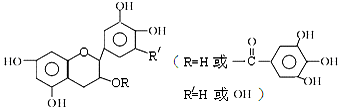
| A. | 儿茶素能与FeCl3溶液发生显色反应 | |
| B. | 1mol儿茶素最多可与10mol NaOH反应 | |
| C. | 常温下,儿茶素不溶于水,也不溶于有机溶剂 | |
| D. | 儿茶素一定不能发生水解反应 |
查看答案和解析>>
科目: 来源: 题型:填空题
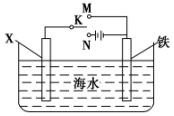 利用如图装置,可以模拟铁的电化学防护.
利用如图装置,可以模拟铁的电化学防护.查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com