
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:解答题
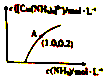 元素铜在溶液中主要以[Cu(H2O)4]2+(天蓝色)、[Cu(OH)4]2-(蓝色)、[CuCl2]-、[Cu(NH3)4]2+(深蓝色)等形式存在.CuCl为难溶于水的白色固体.回答下列问题:
元素铜在溶液中主要以[Cu(H2O)4]2+(天蓝色)、[Cu(OH)4]2-(蓝色)、[CuCl2]-、[Cu(NH3)4]2+(深蓝色)等形式存在.CuCl为难溶于水的白色固体.回答下列问题:查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③⑤ | B. | ③⑤⑥⑦ | C. | ③④⑥⑦ | D. | ②③⑥⑦ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在标况下,22.4LSO3和22.4LC2H4原子个数比为2:3 | |
| B. | 将78gNa2O2与过量CO2反应转移的电子数为2NA | |
| C. | 28g乙烯分子中含有极性共价键的数目为6NA | |
| D. | 1molNaCl晶体中含有NA个Na+ |
查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 空气中的分子质量变大 | B. | 空气中的分子间隔变小 | ||
| C. | 空气中的分子种类改变 | D. | 空气中的分子数目变少 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com