
科目: 来源: 题型:选择题
| A. | NH4+、Ba2+、Br-、CO32- | B. | K+、Na+、SO32-、MnO4- | ||
| C. | Al3+、Na+、AlO2-、Cl- | D. | Na+、Ba2+、Cl-、NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 非金属性:Cl>Br | B. | 酸性:H2SO4>H3PO4 | ||
| C. | 碱性:KOH>NaOH | D. | 热稳定性:Na2CO3<NaHCO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
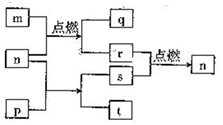 短周期主感元素X、Y、Z、W原子序数依次增大,W2+的电子层结构与氖相同,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种碱性氧化物,它们的关系如图所示( )
短周期主感元素X、Y、Z、W原子序数依次增大,W2+的电子层结构与氖相同,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种碱性氧化物,它们的关系如图所示( )| A. | Y、Z、W的简单离子半径:W>Z>Y | B. | 最高价氧化物的水化物的碱性:Z>W | ||
| C. | 简单气态氢化物的热稳定性:X>Y | D. | Y与Z形成的化合物中不含有共价键 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 | |
| B. | 盐酸可作铁制品的除锈剂 | |
| C. | 实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞 | |
| D. | 将FeCl3饱和溶液滴入沸水中制Fe(OH)3胶体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | (NH4)2SO4=2NH4++SO42- | B. | NaHS?Na++HS${\;}^{_}$,HS-=H++S2- | ||
| C. | Ba(OH)2=Ba2++2OH- | D. | HF?H++F- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | C8H10中只有3种属于芳香烃的同分异构体 | |
| B. | 苯与溴水混合振荡,水层颜色变浅 | |
| C. | 煤经过气化和液化等物理变化可转化为清洁燃料 | |
| D. | 油脂、蛋白质、纤维素均属于高分子化合物,可以发生水解 |
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:解答题
| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7K2=5.6×10-11 |
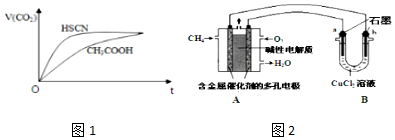
查看答案和解析>>
科目: 来源: 题型:解答题
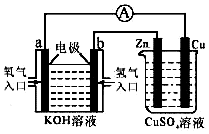 由化学能转变的热能或电能仍然是人类使用的主要能源,根据如图所示的装置,(其中a、b均为石墨电极)
由化学能转变的热能或电能仍然是人类使用的主要能源,根据如图所示的装置,(其中a、b均为石墨电极)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com