
科目: 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,用排水法收集气体 | HX放出的氢气多且反应速率快 | HX酸性比HY强 |
| B | 向2mL 0.1mol/LNa2S溶液中滴2滴0.1mol/LZnSO4溶液;再滴入2滴0.1mol/L CuSO4溶液 | 先生成白色沉淀,后生成黑色沉淀 | 溶度积(Ksp):ZnS>CuS |
| C | 在稀硫酸中加入铜,再加入硝酸钠固体 | 开始无现象,后铜逐步溶解,溶液变蓝,有气泡产生 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 将一铝箔放在酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面生成致密的Al2O3薄膜,且Al2O3熔点高于Al |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 臭氧能用于杀菌消毒 | 臭氧的还原性使细菌的蛋白质变性 |
| B | 铁能用于治疗缺铁性贫血 | 铁能与盐酸生成三氯化铁 |
| C | 过氧化钠作呼吸面具中的供氧剂 | 过氧化钠是强氧化剂,能氧化二氧化碳 |
| D | 用浸有酸性高锰酸钾的硅藻土作水果保鲜剂 | 高锰酸钾能氧化水果释放的催熟剂乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:实验题
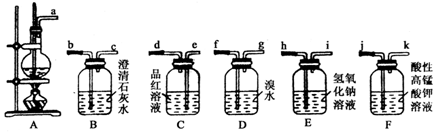
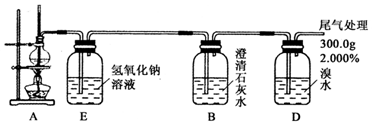
查看答案和解析>>
科目: 来源: 题型:选择题
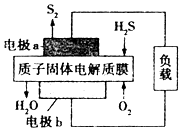 H2S废气资源利用的途径之一是回收并得到S2(g).反应原理为2H2S(g)+O2(g)═S2(g)+2H2O(1)△H=-632kJ•mol-1.如图所示为H2S燃料电池的结构示意图.下列说法正确的是( )
H2S废气资源利用的途径之一是回收并得到S2(g).反应原理为2H2S(g)+O2(g)═S2(g)+2H2O(1)△H=-632kJ•mol-1.如图所示为H2S燃料电池的结构示意图.下列说法正确的是( )| A. | 电池工作时,电子从电极a经质子固体电解质膜流向电极b | |
| B. | 电极a上发生的电极反应为2H2S+4OH--4e-═S2+4H2O | |
| C. | 当电路中通过2 mol电子时,有2 mol H+经质子固体电解质膜进入正极区 | |
| D. | 当反应中生成64 g S2时,电池内部有632KJ的能量转化为电能 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用铂丝蘸取少量无色溶液进行焰色反应 | 火焰呈黄色 | 该溶液是钠盐溶液 |
| B | 向Fe(NO3)2溶液中滴加稀硫酸,再滴加几滴KSCN溶液 | 溶液变红色 | 稀硫酸能氧化Fe(NO3)2 |
| C | 向AgCl悬浊液加入NaI溶液 | 出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| D | 向KI溶液中加入新制氯水和CCl4,C充分振荡、静置 | 液体分层,下层紫红色 | Cl2的氧化性强于I2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 形成简单离子的离子半径为D>C>A | |
| B. | 四种元素形成的简单氢化物中,D的沸点最高 | |
| C. | B的氧化物对应水化物为弱酸,C和D的氧化物对应水化物均为强酸 | |
| D. | C和D形成的某种化合物具有8电子稳定结构,其化学式可能是C2D2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe、A1、Cu均是重要的金属元素,它们的氧化物都是碱性氧化物 | |
| B. | 加热Na2CO3溶液至水分蒸干,可得到NaHCO3和NaOH混合物 | |
| C. | 碳化硅的硬度大、熔点高,是一种高温结构陶瓷 | |
| D. | 工业上用电解熔融MgCl2•6H2O的方法冶炼金属镁 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 误服BaCl2中毒,可服用硫酸钠溶液解毒 | |
| B. | PM2.5颗粒(直径约为2.5×10-6m)分散到空气中形成气溶胶 | |
| C. | 硅可用于制造光电池和高性能的现代通讯材料 | |
| D. | 汽车尾气中含有的氮氧化物是汽油不完全燃烧生成的 |
查看答案和解析>>
科目: 来源: 题型:解答题
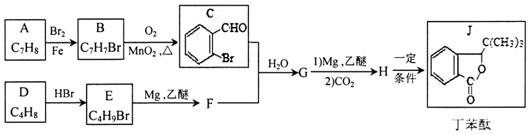
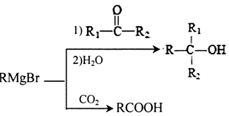
 .H发生缩聚反应生成的高分子化合物的结构简式为
.H发生缩聚反应生成的高分子化合物的结构简式为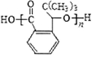 .
.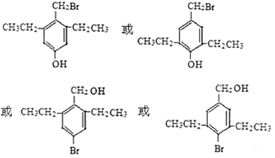 .
.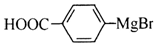 能与CO2反应生成有机物M.符合下列条件的M的同分异构体共有10种.
能与CO2反应生成有机物M.符合下列条件的M的同分异构体共有10种.查看答案和解析>>
科目: 来源: 题型:解答题
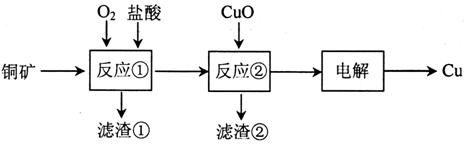
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com