
科目: 来源: 题型:选择题
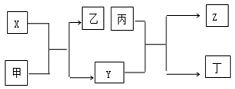 由短周期主族元素X、Y、Z组成的单质(化学式也分别为X、Y、Z),X为金属,其核外电子数为Y原子序数的2倍,Y的最低负化合价与Z的最高正化合价的数值相等,甲、乙、丙、丁四种均为氧化物,甲和丁为无色的气体,固体甲可用于人工降雨,乙和丙熔点均很高,且它们在一定条件下能发生如下反应,下列说法中正确的是( )
由短周期主族元素X、Y、Z组成的单质(化学式也分别为X、Y、Z),X为金属,其核外电子数为Y原子序数的2倍,Y的最低负化合价与Z的最高正化合价的数值相等,甲、乙、丙、丁四种均为氧化物,甲和丁为无色的气体,固体甲可用于人工降雨,乙和丙熔点均很高,且它们在一定条件下能发生如下反应,下列说法中正确的是( )| A. | X为第三周期II族元素,Y和Z位于同一主族 | |
| B. | 甲、乙、丙均能与水发生化合反应 | |
| C. | 工业上常用电解乙制备X | |
| D. | X可用于制焰火烟花,Z可用作太阳能电池的材料 |
查看答案和解析>>
科目: 来源: 题型:解答题
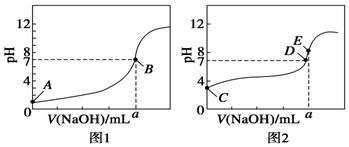 常温下,用0.100 0mol•L-1 NaOH溶液分别滴定20.00mL 0.100 0mol•L-1 HCl溶液和20.00mL 0.100 0mol•L-1 CH3COOH溶液,得到两条滴定曲线,如图所示.
常温下,用0.100 0mol•L-1 NaOH溶液分别滴定20.00mL 0.100 0mol•L-1 HCl溶液和20.00mL 0.100 0mol•L-1 CH3COOH溶液,得到两条滴定曲线,如图所示.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 气体总质量保持不变 | B. | 消耗Z的速率与消耗X的速率相等 | ||
| C. | X、Y、Z的浓度不再发生变化 | D. | X、Y、Z的分子数之比为1:2:2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 150mL1mol/L的氯化钠溶液 | B. | 75mL2mol/L的氯化铵溶液 | ||
| C. | 150mL3mol/L的氯化钾溶液 | D. | 75mL1mol/L的氯化亚铁溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 磷酸与烧碱、硝酸与澄淸石灰水 | |
| B. | 氯化钡与硫酸钠、硫酸与硝酸钡 | |
| C. | 碳酸铵与氢氧化钠、碳酸铵与石灰乳 | |
| D. | 纯碱与硫酸、碳酸氢钾与盐酸 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | SO2能使FeCl3、酸性KMnO4溶液迅速褪色 | |
| B. | 可以用澄清石灰水来鉴别SO2与CO2 | |
| C. | 氨气和酸相遇都能产生白色烟雾 | |
| D. | 在反应NH3++H+=NH4+中,氨失去电子被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com