
科目: 来源: 题型:选择题
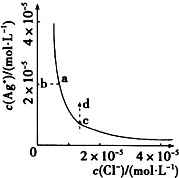 某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )
某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )| A. | d点没有AgCl的不饱和溶液 | |
| B. | c点对应的Ksp 等于a点对应的Ksp | |
| C. | 加入AgNO3,可以使溶液由c点变到d点并保持不变 | |
| D. | 加入少量水,平衡右移,Cl- 浓度减小 |
查看答案和解析>>
科目: 来源: 题型:解答题
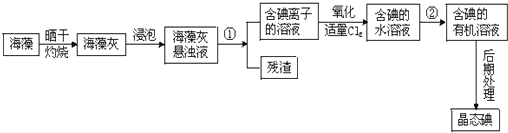
查看答案和解析>>
科目: 来源: 题型:选择题
| 测定时刻/s | t1 | t2 | t3 | t4 |
| c(A)/(mol•L-1) | 6 | 3 | 2 | 2 |
| c(B)/(mol•L-1) | 5 | 3.5 | 3 | 3 |
| c(C)/(mol•L-1) | 1 | 2.5 | 3 | 3 |
| A. | 在t3时刻反应已经停止 | |
| B. | A的转化率比B的转化率低 | |
| C. | t1至t2时刻该反应的速率为3mo1•L-1•s-1 | |
| D. | 该反应的化学方程式为2A(g)+B(g)?C(g) |
查看答案和解析>>
科目: 来源: 题型:填空题
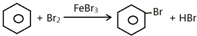 ;
;
查看答案和解析>>
科目: 来源: 题型:解答题
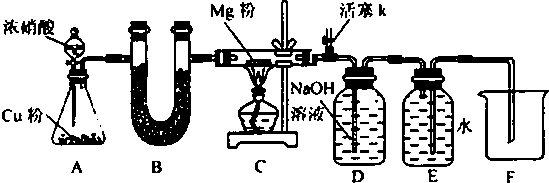
 某化学创新实验小组设计如图示实验装置来制取溴苯并证明该反应为取代反应.已知:溴苯的熔点为?30.8℃,沸点156℃.
某化学创新实验小组设计如图示实验装置来制取溴苯并证明该反应为取代反应.已知:溴苯的熔点为?30.8℃,沸点156℃. ;
;查看答案和解析>>
科目: 来源: 题型:解答题
| 序号 | 实验方案 | 实验现象 | 化学方程式 |
| ① | 将少量氯水加入盛有NaBr溶液的试管中,用力振荡后加入少量四氯化碳溶液,振荡、静置 | 加入氯水后,溶液由无色变为橙色,滴入四氯化碳后,水层颜色变浅,四氯化碳层变为橙红色 | Cl2+2NaBr=2NaCl+Br2 |
| ② | 将少量溴水加入盛有碘化钾溶液的试管中,用力振荡后加入少量四氯化碳溶液,振荡、静置 | 加入溴水后,溶液由无色变为褐色,滴入四氯化碳后,水层颜色变浅,四氯化碳层变为紫红色 |
查看答案和解析>>
科目: 来源: 题型:选择题
| t/min | 0 | 3 | 10 | 12 |
| n(CO)/mol | 2 | 1 | 0.5 | 0.5 |
| n(CH3OH)/mol | 0 | 1 | 1.5 | 1.5 |
| A. | 在0~3min内,用H2表示的平均反应速率为0.33mol•L-1•min-1 | |
| B. | 在该条件下,上述反应的平衡常数为3 | |
| C. | 反应达平衡时,CH3OH (g)的体积分数为50% | |
| D. | 要增大反应速率且增大 CH3OH (g)在混合物中的体积分数,可采用压缩体积,增大体系压强的措施 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 达到平衡时A的总转化率为40% | B. | 达到平衡时c(B)为1.0mol•L-1 | ||
| C. | 达到平衡时c(B)=2c(D) | D. | 达到平衡时c(D)为0.5mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com