
科目: 来源: 题型:多选题
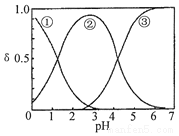 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )| A. | 曲线①代表的粒子是HC2O4- | |
| B. | 0.1mol•L-1NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) | |
| C. | pH=5时,溶液中主要含碳微粒浓度大小关系为:c(C2O42-)>c(H2C2O4)>c(HC2O4-) | |
| D. | 在一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(C2O42-)将减小,c(Ca2+)增大 |
查看答案和解析>>
科目: 来源: 题型:多选题
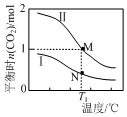 两个容积均为2L的密闭容器Ⅰ和Ⅱ中发生反应:2NO(g)+2CO(g)?N2(g)+2CO2(g),起始物质的量见表.实验测得两容器不同温度下达到平衡时CO2的物质的量如图所示,下列说法正确的是( )
两个容积均为2L的密闭容器Ⅰ和Ⅱ中发生反应:2NO(g)+2CO(g)?N2(g)+2CO2(g),起始物质的量见表.实验测得两容器不同温度下达到平衡时CO2的物质的量如图所示,下列说法正确的是( )| 容器 | 起始物质的量 | |
| NO | CO | |
| Ⅰ | 1 mol | 3 mol |
| Ⅱ | 6 mol | 2 mol |
| A. | N点的平衡常数为0.04 | |
| B. | M、N两点容器内的压强:P(M)>2P(N) | |
| C. | 若将容器Ⅰ的容积改为1 L,T1温度下达到平衡时c(CO2)=0.25 mol•L-1 | |
| D. | 若将容器Ⅱ改为绝热容器,实验起始温度为T1,达平衡时NO的转化率小于16.7% |
查看答案和解析>>
科目: 来源: 题型:选择题
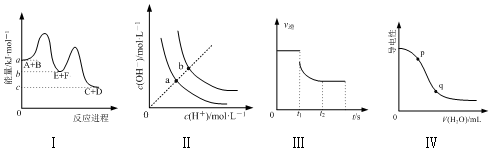
| A. | 图Ⅰ表示反应A+B═C+D的△H=(a-c) kJ•mol-1 | |
| B. | 图Ⅱ表示不同温度下水溶液中H+和OH-的浓度变化曲线,图中a点对应温度高于b点 | |
| C. | 图Ⅲ表示N2+3H2?2NH3的v逆随时间变化曲线,由图知t1时刻可能减小了容器内的压强 | |
| D. | 图Ⅳ表示向醋酸稀溶液中加水时溶液的导电性变化,图中p点pH大于q点 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| 弱酸 | HCOOH | HCN | H2S |
| 电离平衡常数(25℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
| A. | 等体积、等浓度的HCOONa和NaCN两溶液中所含阴离子数目相等 | |
| B. | HCOO-、CN-、HS-在溶液中可以大量共存 | |
| C. | NaHS溶液中加入适量KOH后:c(Na+)═c(H2S)+c(HS-)+C(S2-) | |
| D. | 恰好中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Y、Z、W原子半径依次增大 | |
| B. | X的最高价氧化物对应水化物的酸性比R的强 | |
| C. | X、R分别与Y形成的常见化合物中化学键类型相同 | |
| D. | 元素W、R的简单离子具有相同的电子层结构 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 元素代号 | A | B | D | E | G | I | J | K |
| 化合价 | -1 | -2 | +4 -4 | -1 | +5 -3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
| A. | 常温下B元素的单质能与K单质反应 | |
| B. | A、I、J的离子半径由大到小顺序是A>J>I | |
| C. | G元素的单质存在同素异形体 | |
| D. | J在DB2中燃烧生成B元素的单质 |
查看答案和解析>>
科目: 来源: 题型:推断题
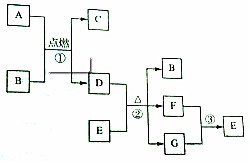 有关物质的转化关系如图所示(部分物质和条件已略去).A是金属单质,D是非金属单质,B、F是气体且B无色无味,G是最常见的无色液体.请回答下列问题:
有关物质的转化关系如图所示(部分物质和条件已略去).A是金属单质,D是非金属单质,B、F是气体且B无色无味,G是最常见的无色液体.请回答下列问题: ;
;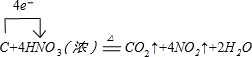 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 10:1 | B. | 9:1 | C. | 1:9 | D. | 1:10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com