
科目: 来源: 题型:选择题
| 选项 | 分子式 | 同分异构体数目 |
| A | CH2F2 | 2种 |
| B | C2H6O | 3种 |
| C | C3H7Cl | 4种 |
| D | C4H8 | 5种 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
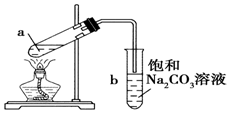
| A. | 向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸 | |
| B. | 试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象 | |
| C. | 实验时加热试管a的目的是加快反应速率并及时将乙酸乙酯蒸出 | |
| D. | 试管b中饱和Na2CO3溶液的作用是吸收随乙酸乙酯蒸出的少量乙酸和乙醇 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | [M+]>[OH-]>[A-]>[H+] | B. | [M+]>[A-]>[H+]>[OH-] | C. | [M+]>[A-]>[OH-]>[H+] | D. | [M+]>[H+]=[A-]>[OH-] |
查看答案和解析>>
科目: 来源: 题型:实验题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 20% | B. | 25% | C. | 30% | D. | 75% |
查看答案和解析>>
科目: 来源: 题型:解答题
 乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用装置来制备.
乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用装置来制备.查看答案和解析>>
科目: 来源: 题型:解答题
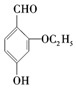 )是食品添加剂的增香原料.
)是食品添加剂的增香原料.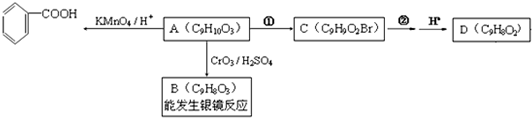
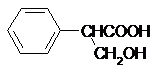 ,B
,B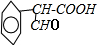 .
.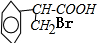 +H2O$→_{△}^{NaOH}$
+H2O$→_{△}^{NaOH}$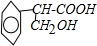 +HBr.
+HBr.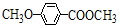 )是一种医药中间体.由茴香醛(
)是一种医药中间体.由茴香醛(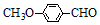 )合成E(其他原料自选),涉及的反应类型有(按反应顺序填写)氧化、酯化.
)合成E(其他原料自选),涉及的反应类型有(按反应顺序填写)氧化、酯化.查看答案和解析>>
科目: 来源: 题型:实验题
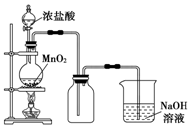 实验室中常用MnO2氧化浓盐酸的方法制取氯气,实验装置如图所示:
实验室中常用MnO2氧化浓盐酸的方法制取氯气,实验装置如图所示:查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:实验题
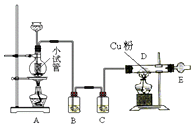 如图是用干燥纯净的Cl2与Cu粉反应来制取无水氯化铜的实验装置图,请回答下列问题:
如图是用干燥纯净的Cl2与Cu粉反应来制取无水氯化铜的实验装置图,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com