
科目: 来源: 题型:实验题
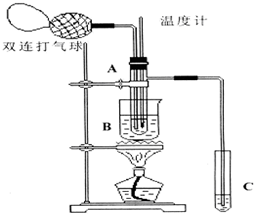 下面是某化学学习小组的同学进行研究性学习的过程,请你参与并协助他们完成相关学习任务.
下面是某化学学习小组的同学进行研究性学习的过程,请你参与并协助他们完成相关学习任务.| 物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| 离子 | K+ | Mg2+ | Ca2+ | NO3- | H2PO4- | SO42- | Zn2+ |
| $\frac{培养液浓度}{nmol•{L}^{-1}}$ | 1 | 0.25 | 1 | 2 | 1 | 0.25 | 1 |
| A. | Zn2+ | B. | SO42- | C. | Ca2+ | D. | H2PO4- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 质量数为18的氧核素:${\;}_8^{18}$O | B. | 锂离子的结构示意图: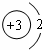 | ||
| C. | 硝基苯的结构简式: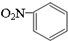 | D. | 四氯化碳的电子式: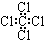 |
查看答案和解析>>
科目: 来源: 题型:实验题
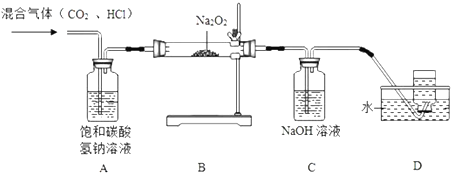
查看答案和解析>>
科目: 来源: 题型:实验题
 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 放电时的Cu为负极 | |
| B. | 充电时电解液的pH升高 | |
| C. | 充电时阳极电极反应为:PbSO4+2H2O-2e-═PbO2+4H++SO42- | |
| D. | 每消耗1molCu,电解质溶液中转移2mol电子 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 0.1mol/LNa2CO3溶液:c(Na+)=2c(H2CO3)+2 c(HCO3-)+c(CO32?) | |
| B. | 能使酚酞溶液呈红色的溶液:Na+、Ba2+、I-、NO3-可以大量共存 | |
| C. | 任何条件下,pH=1的硫酸溶液中:c(H+)=0.1mol/L | |
| D. | 将0.2 mol•L-1的HCN溶液和0.1 mol•L-1的NaOH溶液等体积混合,溶液显碱性,则c(HCN)=c(CN-)=c(Na+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com