
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 等于0.1mol/L | B. | 大于0.1mol/L | C. | 小于0.1mol/L | D. | 无法判断 |
查看答案和解析>>
科目: 来源: 题型:选择题
 ,关于有机物A的说法不正确的是( )
,关于有机物A的说法不正确的是( )| A. | A的分子式为C16H14O3 | |
| B. | A可使酸性KMnO4溶液和溴水褪色 | |
| C. | A苯环上的一氯代物同分异构体有2种 | |
| D. | A既可发生氧化反应和加成反应,也可以发生取代反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯乙烯和溴乙烷均能发生加成反应 | |
| B. | 花生油和玉米油都是可皂化的饱和酯类 | |
| C. | 天然气和水煤气的主要成分都是烃类 | |
| D. | 分子式为C10H14的单取代芳烃,其可能的结构有4种 |
查看答案和解析>>
科目: 来源: 题型:选择题
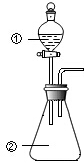 用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( ) | 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 浓盐酸 | MnO2 | 产生黄绿色气体 |
| B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C | 酸化的FeCl2溶液 | H2O2溶液 | 溶液变成黄棕色,有气泡产生 |
| D | Fe2(SO4)3溶液 | 铜粉 | 溶液变蓝色,有黑色固体产生 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
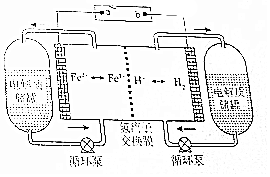 H2-Fe3+/Fe2+氧化还原液流电池是一种新型氧化还原液流电池,电池的结构如图所示,电解质溶液为1 mol/L H2SO4和0.5 mol/L Fe2(SO4)3的混合液.下列说法正确的是( )
H2-Fe3+/Fe2+氧化还原液流电池是一种新型氧化还原液流电池,电池的结构如图所示,电解质溶液为1 mol/L H2SO4和0.5 mol/L Fe2(SO4)3的混合液.下列说法正确的是( )| A. | 充电时,a连接直流电源的正极 | |
| B. | 充电时,阴极的电极反应式为2Fe3++2e-═2Fe2+ | |
| C. | 放电时,右侧电解质储罐中的SO42-浓度逐渐增加 | |
| D. | 放电时,当转移0.1mol e-时,透过交换膜的离子有0.2mol |
查看答案和解析>>
科目: 来源: 题型:选择题
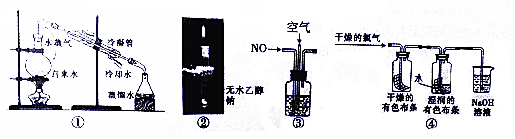
| A. | 图①用于除去自来水中的Fe3+、C1-等杂质离子 | |
| B. | 图②中直接点燃气体,证明钠与乙醇反应的气体产物是H2 | |
| C. | 图③在探究NO充分转化成HNO3的实验中,观察气泡速率控制通入气体体积比 | |
| D. | 图④用该实验可以证明Cl2体现漂白作用的原因 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | W与氢形成的原子比为1:1的化合物有多种 | |
| B. | X的氢化物只含有极性共价键 | |
| C. | Y单质可通过电解Y的氯化物获得 | |
| D. | W与Z形成化合物WZ2中各原子均满足8电子稳定结构 |
查看答案和解析>>
科目: 来源: 题型:解答题
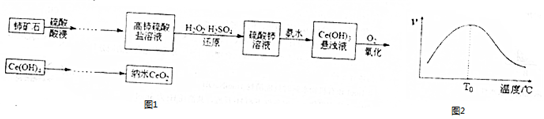
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将0.4mol/LNH4Cl溶液和0.2molNaOH溶液等体积混合后,溶液中粒子的物质的量浓度大小关系为:c(NH4+)>c(Na+)>c(NH3•H2O)>c(OH-)>c(H+) | |
| B. | SiO2(s)+2C(s)═Si(s)+2CO(g)在常温下不能自发进行,则该反应的△H>0 | |
| C. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合后的溶液中:2c(Na+)═c(CH3COO-)+c(CH3COOH) | |
| D. | 在相同条件下,NaHCO3溶液和NaHSO3溶液中,水的电离平衡均被促进 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com